Artículo de la Práctica Clínica
Caracterización epidemiológica, clínica y micológica de neonatos graves con candidemia por complejo Candida parapsilosis
Epidemiological, clinical and mycological characterization of severely ill neonates with candidemia due to Candida parapsilosis complex
Liena González Lorenzo1* https://orcid.org/0000-0003-0064-1344
Dianiley García Gómez1 https://orcid.org/0000-0001-9572-5570
Calixta Rosa Hernández del Sol1 https://orcid.org/0000-0001-8403-1426
Mayda Rosa Perurena Lancha2 https://orcid.org/0000-0002-5255-9012
Yisel González Madariaga3 https://orcid.org/0000-0002-0461-0741
1Hospital Provincial Gineco-obstétrico Universitario “Mariana Grajales”. Villa Clara, Cuba.
2Instituto de Medicina Tropical “Pedro Kourí”. La Habana, Cuba.
3Universidad de Ciencia Médicas de Villa Clara. Villa Clara, Cuba.
*Autor para la correspondencia. Correo electrónico: lienagl@infomed.sld.cu
RESUMEN
Introducción: El complejo Candida parapsilosis representa una grave amenaza para los neonatos, con un incremento en la resistencia a los antimicóticos utilizados para el tratamiento.
Objetivo: Caracterizar la epidemiología, clínica y micología de los neonatos graves con candidemia por el complejo C. parasilosis.
Métodos: Estudio observacional, descriptivo y transversal, de neonatos hospitalizados en unidades de atención al grave de 2 instituciones provinciales, en el período entre mayo de 2022 hasta diciembre de 2024. Se analizaron las variables epidemiológicas: Sexo del paciente, mes, estaciones del año y hospital; micológicas: Sensibilidad y resistencia a los antifúngicos probados. Se calcularon frecuencias absolutas y porcentajes.
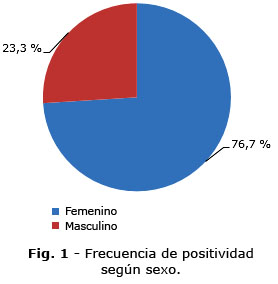
Resultados: De los 30 neonatos con candidemia por complejo C. parapsilosis, el 76,7 % correspondieron al sexo femenino. Abril fue el mes más representativo con 11 aislados seguido de diciembre con 4. El 66,7 % de las infecciones ocurrieron entre noviembre y abril, tiempo que corresponde a los meses más fríos y las féminas el grupo poblacional más afectado. El 26,7 % de los pacientes fallecieron y de estos, el 62,5 % pertenecían al Hospital Gineco-obstétrico, con igualdad de género en ambas instituciones. Los mayores niveles de sensibilidad correspondieron a la anfotericina B (90 %).
Conclusiones: Predominaron los neonatos del sexo femenino con candidemia diagnosticada fundamentalmente en la estación de invierno; a pesar de la elevada mortalidad, prevalecieron los aislados clínicos sensibles a la anfotericina B.
Palabras clave: Candida parapsilosis; candidemia; neonatos.
ABSTRACT
Introduction: Candida parapsilosis complex represents a serious threat to newborns, with an increase in resistance to antifungal sused for treatment.
Objective: To characterize the epidemiology, clinical symptoms and mycology of critically ill neonates with candidemia due to the C. parasilosis complex.
Methods: An observational, descriptive, cross-sectional study of newborns hospitalized in acute care units at two provincial institutions from May 2022 to December 2024. Epidemiological variables were analyzed, including patient sex, month, season and hospital; and mycological variables included sensitivity and resistance to antifungal tested. Absolute frequencies and percentages were calculated.
Results: Of the 30 newborns with candidemia due to C. parapsilosis complex, 76.7% were female. April was the most representative month with 11 isolates, followed by December with four. 66.7% of infections occurred between November and April, which corresponds to the coldest months, and women are the most affected population group. 26.7% of patients died, and of these, 62.5% were from the Gynecological-obstetric Hospital, with gender equality in both institutions. The highest levels of susceptibility were to amphotericin B (90%).
Conclusions: Female neonates with candidemia, diagnosed primarily during the winter season, predominanted; despite the high mortality rate, clinical isolates sensitive to amphotericin B prevailed.
Keywords: Candida parapsilosis; candidemia; infant, newborn.
Recibido: 13/05/2025
Aprobado: 20/08/2025
INTRODUCCIÓN
Las especies de Candida son causa importante de morbimortalidad en los recién nacidos hospitalizados, con riesgo de secuelas graves, que incluyen daño neurológico, afectación visual, auditiva y displasia broncopulmonar.(1)
Los índices de incidencia de candidiasis invasiva neonatal (CIN) de forma global varían y están asociados a una elevada mortalidad, que van desde un 12 % a 37 % en los países de altos ingresos económicos y de 9 % a 75 % en los de medianos y bajos ingresos.(2)
El complejo Candida parapsilosis es la segunda especie de Candida más aislada en hemocultivos en el sur de Europa, Latinoamérica y Asia.(1,3) Está incluida en la primera lista de patógenos fúngicos prioritarios de la Organización Mundial de la Salud, con el objetivo de darle vigilancia sistemática, teniendo en cuenta las necesidades de investigación y desarrollo no satisfechas y la importancia percibida para la salud pública.(4)
Dentro de las especies de Candida, este complejo representa una grave amenaza para los recién nacidos, especialmente los prematuros y con bajo peso al nacer, los cuales pueden adquirir la infección y colonización de la piel, tracto gastrointestinal y las vías respiratorias desde el paso por el canal de parto.(1,5,6,7) Además, es capaz de colonizar catéteres intravasculares y las manos de los trabajadores de salud; crece rápidamente en soluciones de nutrición parenteral con alto contenido de glucosa y facilita el desarrollo de brotes de infecciones intrahospitalarias.(1,5,6,7)
Aunque inicialmente estas especies de Candida se consideraron susceptibles al fluconazol, antimicótico más utilizado para el tratamiento, actualmente un número creciente de países diagnostican resistencia a dicho fármaco. Esta situación pone en peligro las estrategias de tratamientos basadas en “azoles” e incrementa los índices de mortalidad en pacientes con enfermedad invasiva.(2,7)
Un estudio(8) de candidemia realizado en Villa Clara entre los años 2009 al 2018 en el que se incluye el servicio de Neonatología, informa predominio de Candida tropicalis y otras especies, con escasos aislados de C. parasilosis. Cuatro años más tarde, otra investigación(9) en esta provincia ya reporta al complejo C. parasilosis como la especie más frecuente responsable de la candidemia con 41 aislados para un 80 %. Los datos referidos evidencian un incremento en el diagnóstico de estas especies.
El objetivo de esta investigación es realizar una caracterización epidemiológica, clínica y micológica de los neonatos graves con candidemia por el complejo C. parasilosis.
MÉTODOS
Diseño
Se realizó un estudio observacional descriptivo y transversal, de una serie de casos de neonatos hospitalizados en unidades de atención al grave.
Sujetos
La serie estuvo conformada por 30 neonatos con diagnóstico de candidemia por complejo C. parapsilosis, con más de 2 días de hospitalización, sin tratamiento previo con antifúngicos, atendidos en el período comprendido entre mayo de 2022 hasta diciembre de 2024, en 2 instituciones provinciales: Hospital Provincial Gineco-obstétrico Universitario “Mariana Grajales” y Hospital Provincial Pediátrico Universitario “José Luis Miranda”, ambos de Villa Clara. La evaluación clínica para incluir al recién nacido en el estudio fue efectuada por especialistas en Neonatología.
Variables
Se analizaron las variables epidemiológicas como: Sexo del paciente, mes, estaciones del año y hospital; micológicas: Sensibilidad y resistencia a los antifúngicos probados. Se consideró neonato al paciente de 0 a 28 días de nacido.
Procedimientos
Los especialistas en Microbiología garantizaron el control de la calidad, en cada etapa de trabajo para el diagnóstico microbiológico y minimizar el sesgo en el procesamiento de las muestras clínicas. Se tomó sangre, entre 0,5-1 mL de cada brazo del neonato; ejecutada por el personal de enfermería. Se inoculó en frascos con medios de cultivos en caldo proporcionados por CPM Scientifica (Italia), se incubaron a 36 ± 1 0C por 48 horas y después se realizó un subcultivo en agar dextrosa Sabouraud con cloranfenicol.
La identificación y pruebas de susceptibilidad se realizaron en 2 momentos. El primero comprendió desde mayo de 2022 a mayo de 2024, en el Laboratorio Nacional de Referencia de Micología del Instituto de Medicina Tropical “Pedro Kourí” (LNR-M del IPK); el segundo, desde junio a diciembre de 2024, en el Laboratorio de Microbiología del Hospital Provincial Gineco-obstétrico Universitario “Mariana Grajales”.
Cultivo e identificación de levaduras
En el Laboratorio de Microbiología del Hospital Provincial Gineco-obstétrico Universitario “Mariana Grajales”, el subcultivo en agar dextrosa Sabouraud con cloranfenicol se incubó a 28 0C durante 15 días. Al lograr el crecimiento de colonias con macromorfología sugestiva de levaduras se identificaron por examen microscópico directo con tinción de Gram.
Prueba del tubo germinativo
Se realizó la prueba de formación de tubo germinativo a cada aislado, según la técnica descrita por McGinnis MR.(10) Se utilizó 0,5 mL de clara de huevo como medio elaborado de forma estéril y dispensada en viales de 1,5 mL. Se utilizaron C. albicans ATCC 90028 y C. parapsilosis ATCC 22019 como controles positivo y negativo, respectivamente. Las muestras en las cuales se observó tubos germinativos se informaron como complejo C. albicans y en los negativos, se prosiguió con las pruebas de identificación. Los aislados clínicos se enviaron al LNR-M del IPK para continuar con su diagnóstico fenotípico.
Zimograma
Se realizó prueba de fermentación de azúcares (glucosa, sacarosa, maltosa, lactosa, galactosa y rafinosa) según la metodología de McGinnis MR,(10) cuando la técnica de formación de tubo germinativo resultó negativa.
Filamentación en agar harina de maíz + Tween 80
En el LNR-M del IPK, se continuó el diagnóstico mediante la filamentación en agar harina de maíz + Tween 80 en placas de Petri (técnica de Dalmau), a partir de los aislados clínicos recibidos en viales con agua destilada estéril. A las 48 horas de incubación, se examinaron al microscopio en busca de los patrones característicos de crecimiento, como pseudohifas o hifas verdaderas y clamidosporas terminales e intercalares.
API 20 C AUX
Se utilizó el sistema comercial API 20 C AUX (bioMérieux, Marcy, l´Étoile, Francia)(11) para los aislados diferentes del complejo C. albicans, para evaluar la capacidad de asimilación de carbohidratos según las recomendaciones del fabricante.
Determinación de la susceptibilidad a los antifúngicos in vitro
Se comprobó in vitro con el ATB™ Fungus 3 (bioMérieux, Marcy, l´Étoile, Francia),(11) por valores de concentración mínima inhibitoria (CMI). Se investigaron 2 antifúngicos con diferentes concentraciones: Anfotericina B (AMB): 0,5; 1; 2; 4; 8 y 16 μg/mL y fluconazol (FCA): 1; 2; 4; 8; 16; 64 y 128 μg/mL.
Las concentraciones críticas empleadas para dar el criterio de sensible, intermedio o resistente al FCA, fueron tomadas de los métodos de referencia de dilución en caldo, para determinar la susceptibilidad de levaduras de importancia clínica propuestos por el Instituto de Estándares Clínicos y de Laboratorios de EE. UU.(CLSI), 2022.(12) Para AMB se tomaron los puntos de corte epidemiológicos (PCE) establecidos por Pfaller MA y otros,(13) en la que la CMI ≤ 1 se consideró sensible y la CMI > 1 resistente.
Procesamiento
Los datos fueron procesaron por medio de los programas IBM SPSS versión 22 y Microsoft Excel 2016. Se calcularon frecuencias absolutas y porcentajes. Los resultados se presentan en tablas y figuras. La estacionalidad se distribuyó en las dos estaciones que comprende Cuba. Los meses de noviembre a abril correspondieron a invierno y de mayo a octubre, verano.
Aspectos bioéticos
Se cumplieron las normas éticas y los principios bioéticos de autonomía, beneficencia, no maleficencia y justicia según la 75th Asamblea Mundial de Helsinki, 2024.(14) Se efectuó la investigación después de ser aprobada por el Comité Científico, el Comité de Ética y las autoridades sanitarias de la institución. La realización de hemocultivos en las unidades de cuidados intensivos de Neonatología está incluida en el protocolo diagnóstico de actuación.
RESULTADOS
De los 30 neonatos graves hospitalizados con candidemia por el complejo C. parapsilosis, el 76,7 % (n= 23) eran del sexo femenino (Fig. 1).
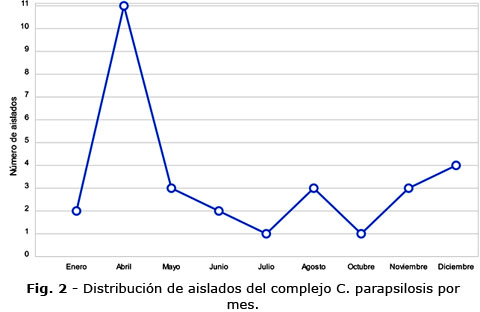
En la figura 2 se muestra la distribución de los aislados clínicos del complejo C. parapsilosis por mes. Abril fue el más representativo con 11 (36,7 %) seguido de diciembre con 4 (13,3 %) y los meses de mayo, agosto y noviembre con 3 (10 %) en cada uno.
En la tabla 1 se ejemplifica la distribución de aislados clínicos por sexo y estaciones del año. La mayoría de las infecciones ocurrieron entre noviembre y abril, que corresponde a los meses más fríos (20; 66,7 %) y el sexo femenino, el grupo más afectado (15; 50 %).
En la tabla 2 se refleja la frecuencia de fallecidos, para un total de 8 (26,7 %) pacientes, distribuidos según hospital y sexo. De estos, 5 (62,5 %) pertenecieron al Hospital Provincial Gineco-obstétrico Universitario “Mariana Grajales” (materno) y 3 (37,5 %) del Hospital Provincial Pediátrico Universitario “José Luis Miranda” (infantil). Hubo igualdad de género en ambas instituciones (50 %); el sexo femenino, en el Hospital Gineco-obstétrico representó el 50 %.
En la tabla 3 se muestra la susceptibilidad a los antifúngicos in vitro en el complejo C. parapsilosis. Ambos fármacos se mostraron activos ante los aislados clínicos. El mayor nivel de sensibilidad correspondió a la anfotericina B con 90 %. En cuanto a la resistencia, solo hubo un 13,3 %, al fluconazol.
DISCUSIÓN
Se constató predominio de pacientes afectados en el sexo femenino. Otras investigaciones(8,9) realizadas en Villa Clara coinciden con estos resultados y señalan mayor frecuencia del sexo femenino. La mayoría de los trabajos revisados difieren de estos resultados y reportan al sexo masculino como el más frecuente.(1,2) Incluso, señalan que desde la etapa fetal, el sistema inmunológico en los varones se compromete desfavorablemente, con repercusión en la etapa neonatal que a su vez constituye un factor de riesgo para la candiduria. Señalan que aún no están bien esclarecidos, los mecanismos de la epigenética, que involucran la aparición de enfermedades neonatales moduladas por el sexo.(15,16,17)
Es opinión de los autores de esta investigación que la incidencia de infecciones micóticas puede variar según el entorno y que factores de riesgo como: La prematuridad, exposición a ambientes hospitalarios y el uso de terapia antimicrobiana juegan un papel decisivo en el desarrollo de las candidemias.
La relación entre candidemia y estaciones del año no está completamente clara. Las más cálidas y húmedas pueden favorecer el crecimiento de hongos, como las levaduras, e influir en los cambios en la flora microbiana hospitalaria, que pueden incrementar el riesgo de infecciones neonatales y nosocomiales. En este estudio se destacó la aparición de candidemia en neonatos, en los meses de noviembre a abril, que se corresponde con la estación de invierno.
Lona JC y otros,(1) en un estudio de incidencia y factores de riesgo asociados a candidiasis invasiva, en una unidad de cuidados intensivos neonatales en México, durante 5 años, informan que la mayoría de las infecciones por Candida (83,5 %; n= 71) ocurren con un patrón entre abril y octubre, tiempo que corresponde a los meses más cálidos del año, resultado que difiere del presente estudio.
Los autores de esta investigación tienen experiencia en el tema abordado con una tesis no publicada de la especialidad de Microbiología; demuestran que la evolución temporal de la candidemia en niños hospitalizados en servicios de atención al grave en Villa Clara no tiene un patrón estacional bien definido. En el invierno puede haber un aumento en la admisión de pacientes en los hospitales, debido a enfermedades respiratorias, lo que puede incrementar el uso de antibióticos y dispositivos médicos invasores, unido al riesgo de infecciones por Candida. Son necesarias más investigaciones sobre los efectos específicos del clima y los eventos climáticos extremos en las candidiasis, para establecer vínculos directos y comprender los mecanismos involucrados.(18)
Farnaz D y otros,(7) hacen referencia a varios estudios realizados en todo el mundo y reafirman que el complejo C. parapsilosis es uno de los microorganismos más comunes que causan candidemia potencialmente mortal en recién nacidos. Desde el 2018 se informan brotes graves causados por cepas resistentes al fluconazol, los cuales se asocian con altas tasas de mortalidad y que pueden persistir a pesar de las estrictas estrategias de control de infecciones.
En esta investigación, el complejo C. parasilosis mostró un elevado índice de mortalidad en recién nacidos. Farnaz D y otros,(7) en su estudio sobre la aparición mundial de Candida parapsilosis resistentes al fluconazol, informan índices de letalidad variables, en un 25 % en neonatos, lo que coincide con los hallazgos de este estudio. Otros autores, como García D y otros(9) y Caparó E y otros(19) difieren al informar índices más elevados con un 84,6 % y un 68 % respectivamente.
El complejo C. parapsilosis presenta múltiples factores de virulencia que pueden influir en la gravedad de la enfermedad. Incluyen características bioquímicas y procesos metabólicos como la producción de fosfolipasas, la síntesis y almacenamiento de ácidos grasos, gran afinidad por superficies sintéticas (mayor que Candida albicans) y diferencias en la estructura y composición de las biopelículas, que confieren protección contra los fármacos antimicóticos y la respuesta inmunitaria del huésped.(7,20) Además, la formación de biopelículas es uno de los sistemas por los cuales los hongos sobreviven en el ambiente y facilitan las infecciones nosocomiales. Se adiciona a estos factores, la aparición de cepas multirresistentes, que contribuyen a mayor incidencia y letalidad de dichas especies, comparadas con las otras.(7,19,20)
Los patrones de resistencia varían de un lugar a otro y aunque estudios multinacionales han demostrado que aún no ha surgido una resistencia generalizada a los antimicóticos, los datos locales pueden mostrar lo contrario.(3) Históricamente, C.parapsilosis será conocido como susceptible al fluconazol. Farnaz D y otros,(7) en una investigación sobre la aparición mundial de Candida parapsilosis resistente a fluconazol muestran que antes del año 2010, rara vez se registraron algunos aislamientos resistentes y señalan el aumento en el comportamiento de la resistencia de más del 10 % entre el período de 2010 y el 2019.
En los últimos años los aislados de C. parapsilosis resistentes al fluconazol se expandieron y superaron a los sensibles en algunos entornos de atención médica; persisten en varios nichos hospitalarios, donde pueden causar brotes esporádicos entre pacientes sin tratamiento con “azoles”, a pesar de la aplicación de estrictas estrategias de control de infecciones.(7)
Las pruebas de susceptibilidad realizadas en esta investigación mostraron una baja resistencia al fluconazol y a la anfotericina B. Con relación al fluconazol, resultados similares son enunciados por Lemus D y otros,(21) con porcentajes de sensibilidad de 87 %. Escribano C y otros(3) informan de un hallazgo semejante en un estudio reciente sobre aislamientos de Candida spp. en hemocultivos recogidos en 16 hospitales ubicados en el área metropolitana de Madrid (2019 a 2021), con 13,6 % de resistencia al fluconazol en C. parapsilosis.
Un estudio de CIN(2) en países de ingresos bajos y medianos da a conocer una alta resistencia de C. parasilosis al fluconazol, con 59 % (19/32), aunque el 90 % de los aislados corresponden a Sudáfrica. Este porcentaje de resistencia es muy superior a los de la presente investigación.
Una publicación regional de Latinoamérica(22) informa resistencia de C. parasilosis al fluconazol de forma global, de 5,7 %. Se manifestó en 7 países (Argentina, Brasil, Chile, Colombia, Perú, Paraguay y Venezuela) de los 10 que informaron estudios de sensibilidad para esta especie, con un rango que varió desde 1,1 hasta 26,9 %. Colombia fue el país más afectado.
Escribano C y otros,(3) plantean que en España las especies aisladas de C. parapsilosis muestran elevada resistencia al fluconazol. Durante los años 2019 al 2021 las tasas aumentaron significativamente en 3,8 % en 2019, 5,7 % en 2020 y 29,1 % en 2021. Informan que menos del 20 % de los pacientes con aislados resistentes al fluconazol habían recibido tratamiento previo con este fármaco, lo que respalda el hecho de que, aunque el fluconazol puede ser un factor clave para promover la resistencia, el principal impulsor que promueve la propagación es la transmisión de paciente a paciente.
La resistencia de C. parasilosis a la anfotericina B según los reportes de la literatura se corresponde en la mayoría, con porcentajes más bajos de resistencias que los encontrados en esta investigación. Cook A y otros,(2) en un estudio multicéntrico informa 93 % de sensibilidad; Lemus D y otros,(21) en Venezuela, 100 %. En un estudio regional en Latinoamérica, realizado por Sanmartín LM y otros,(22) notifican resistencia a la anfotericina B solo en 2 países: Brasil con 5 % y Perú con 7 %.
El seguimiento continuo de la resistencia a los antifúngicos es importante, ya que estas tendencias pueden tardar muchos años en detectarse. En los lugares en que se utiliza fluconazol de forma rutinaria para la profilaxis, se debe realizar un seguimiento sistemático para determinar si los aislados de C. parapsilosis y otras Candida spp. desarrollan resistencia a este fármaco, que continúa siendo el tratamiento antifúngico de elección en los países de ingresos bajos y medianos.
Predominaron los neonatos del sexo femenino con candidemia diagnosticada fundamentalmente en la estación de invierno; a pesar de la elevada mortalidad, prevalecieron los aislados clínicos sensibles a la anfotericina B.
REFERENCIAS BIBLIOGRÁFICAS
1. Lona Reyes JC, Gómez Ruiz LM, Cordero Zamora A, Cortés González SI, Quiles Corona M , Pérez Ramírez RO, et al. Incidencia y factores asociados a candidiasis invasiva en una unidad de cuidados intensivos neonatales de México [Internet]. In Anales de Pediatría. 2022; 97:79-86. DOI: 10.1016/j.anpedi.2021.07.001
2. Cook A, Ferreras L, Adhisivam B, Ballot D, Berkley JA, BernaschiP, et al. Neonatal invasive candidiasis in low- and middle-income countries: Data from the NeoOBS study [Internet]. Medical Mycology. 2023; 61(3): myad010. DOI: 10.1093/mmy/myad010
3. Escribano P, Guinea J. Fluconazole-resistant Candida parapsilosis: A new emerging threat in the fungi arena [Internet]. Front Fungal Bio. 2022; 3: 1010782. DOI: 10.3389/ffunb.2022.1010782
4. WHO. Fungal priority pathogens list to guide research, development and public health action [Internet]. Geneva: World Health Organization; 2022. [acceso: 01/02/2025]. Disponible en: https://www.who.int/publications/i/item/9789240060241
5. Tortorano AM, Prigitano A, Morroni G, Brescini, Barchiesi L. Candidemia: Evolution of Drug Resistance and Novel Therapeutic Approaches [Internet]. Infection and drug resistan. 2021; 14:5543-53. DOI: 10.2147/IDR.S274872
6. Zuo XS, Liu Y, Hu K. Epidemiology and risk factors of candidemia due to Candida parapsilosis in an intensive care unit [Internet]. Rev Inst Med Trop Sao Paulo. 2021; 63:e20. DOI: 10.1590/S1678-9946202163020
7. Farnaz D, João NAJ, Macit I, Lombardi L, Perry MA, Gao M, et al. Worldwide emergence of fluconazol-resistant Candida parapsilosis: current framework and future research roadmap [Internet]. The Lancet Microbe. 2023; 4(6):E470–E480. DOI: 10.1016/S2666-5247(23)00067-8
8. González Lorenzo L, García Gómez D, Castro Martínez JA, López Pérez M, Truffín Truffín EG. Comportamiento de Candida en niños hospitalizados en unidades de cuidados intensivos [Internet]. Medicentro Electrónica. 2023 [acceso: 02/02/2025]; 27(1):e3829. Disponible en: http://scielo.sld.cu/scielo.php?pid=S1029-30432023000100003&script=sci_arttext&tlng=en
9. García Gómez D, Perurena Lancha MR, Choy Marrero A, López Pérez M, Ilnait Zaragozí MT. Características clínicas y micológicas de pacientes hospitalizados con candidemia [Internet]. Rev Cubana Med Milit. 2024 [acceso: 05/04/2025]; 53(4):e58713. Disponible en: https://revmedmilitar.sld.cu/index.php/mil/article/view/5871
10. McGinnis MR. Laboratory Handbook of Medical Mycology [Internet]. New York: Academy Press INC;2012. [acceso: 01/02/2025]. Disponible en: https://shop.elsevier.com/books/laboratory-handbookof-medical-mycology/mcginnis/978-0-12-482850
11. Biomérieux. Manual del Sistema Comercial de Determinación de Susceptibilidad Antifúngica en Levaduras ATB TM FUNGUS 3 [Internet]. Francia: bioMérieux SA; 2008. [acceso: 01/02/2025]. Disponible en: https://www.biomerieux.es/sites/subsidiary_es/files/biom_clinica_2023_esp_ver_sp.pdf
12. CLSI. Performance Standards for Antifungal Susceptibility Testing of Yeats [Internet]. 3rd ed. CLSI supplement M27M44S. Clinical Laboratory Standards Institute; 2022. [acceso: 01/02/2025]. Disponible en: https://clsi.org/standards/products/microbiology/documents/m27m44s/
13. Pfaller MA, Espinel-Ingroff A, Canton E, Castanheira M, Cuenca-Estrella M, Diekema DJ, et al. Wild-Type MIC Distributions and Epidemiological Cutoff Values for Amphotericin B, Flucytosine, and Itraconazole and Candida spp. as Determined by CLSI Broth Microdilution [Internet]. J Clin Microbiol. 2012;50(6):2040-6. DOI: 10.1128/jcm.00248-12
14. World Medical Association. Declaration of Helsinki. Ethical Principles for Medical Research Involving Human Participants [Internet]. JAMA. 2024; 23(18):e21972. DOI: 10.1001/jama.2024.21972
15. Tamayo Pérez VI, Morilla Guzmán AA. Epigenética, sexo masculino y enfermedades neonatales [Internet]. Rev Cubana Pediatr. 2021 [acceso: 13/04/2025]; 93(4):1-19. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S003475312021000400013&lng=es
16. Escribano García C, Montejo Vicente MM, Izquierdo Caballero R, Samaniego Fernández CM, Marín Uruena SI, Infante López ME, et al. Observación clínica de recién nacidos con factores de riesgo infeccioso, una práctica segura [Internet]. An Pediatr (Barc). 2018; 88(5):239-45. DOI: 10.1016/j.anpedi.2017.05.003
17. Tekola-Ayele F, Workalemahu T, Gorfu G, Shrestha D, Tycko B, Wapner R, et al. Sex differences in the associations of placental epigenetic aging with fetal growth [Internet]. Aging (Albany NY). 2019; 11(15):5412–32. DOI: 10.18632/aging.102124
18. Gadre A, Enbiale W, Andersen LK, Coates SJ. The effects of climate change on fungal diseases with cutaneous manifestations: A report from the International Society of Dermatology Climate Change Committee [Internet]. The Journal of Climate Change and Health. 2022; 6:2667-782. DOI: 10.1016/j.joclim.2022.100156
19. Caparó IE, Vásquez VM, Noreroa X, Sáez LX, De Antonio R, Rodríguez BE. Risk factors and lethality associated with neonatal candidemia in a neonatal unit [Internet]. Rev Chil Pediatr. 2019; 90(2):186-93. DOI: 10.32641/rchped.v90i2.717
20. Miyake A, Gotoh K, Iwahashi J, Togo A, Horita, R, Miura M. Characteristics of biofilms formed by C. parapsilosis causing an outbreak in a neonatal intensive care unit [Internet]. Journal of Fungi. 2022; 8(7):700. DOI:10.3390/jof8070700
21. Lemus Espinoza D, Maniscalchi MT. Revisión del perfil de sensibilidad de levaduras aisladas en pacientes del estado Anzoátegui, Venezuela, 2009-2017 [Internet]. Saber. 2021; 33:115-21. DOI: 10.5281/zenodo.5813223
22. Sanmartín Sagbay LM, Espinoza Loja CR, Prieto Fuenmayor CF. Fármacorresistencia en Especies de Candida sp. Causantes de Infecciones Fúngicas Invasivas en Latinoamérica Revisión Sistemática [Internet]. Ciencia Latina. 2024; 8(1):1163-98. DOI: 10.37811/cl_rcm.v8i1.9499
Conflictos de interés
No existen conflictos de interés en relación con la investigación presentada.
Información financiera
No recibieron financiación para la realización de este trabajo.
Contribuciones de los autores
Conceptualización: Liena González Lorenzo, Dianiley García Gómez, Calixta Rosa Hernández del Sol.
Curación de datos: Liena González Lorenzo, Dianiley García Gómez, Calixta Rosa Hernández del Sol.
Análisis formal: Liena González Lorenzo, Dianiley García Gómez, Calixta Rosa Hernández del Sol.
Investigación: Liena González Lorenzo, Dianiley García Gómez, Mayda Rosa Perurena Lancha.
Metodología: Liena González Lorenzo, Dianiley García Gómez. Calixta Rosa Hernández del Sol.
Administración de proyecto: Liena González Lorenzo.
Recursos: Mayda Rosa Perurena Lancha.
Supervisión: Yisel González Madariaga.
Visualización: Liena González Lorenzo, Dianiley García Gómez, Calixta Rosa Hernández del Sol.
Redacción – preparación del borrador original: Liena González Lorenzo, Dianiley García Gómez, Calixta Rosa Hernández del Sol.
Redacción: revisión y edición: Liena González Lorenzo, Dianiley García Gómez. Calixta Rosa Hernández del Sol, Yisel González Madariaga.
Disponibilidad de datos
Archivo complementario: Base de datos de investigación. Excel 2016. Disponible en: https://revmedmilitar.sld.cu/index.php/mil/libraryFiles/downloadPublic/95