Revisión Sistemática
Factores predictivos de recurrencia de fibrilación auricular paroxística tras ablación por catéter
Predictive factors for recurrent paroxysmal atrial fibrillation after catheter ablation
Yoander Nápoles-Zaldivar1* https://orcid.org/0000-0002-9827-6747
Ivonne María Nodarse-Palacios1 https://orcid.org/0000-0002-4436-2041
Edilio Silva-Velasco2 https://orcid.org/0000-0003-1151-6769
1Universidad de Ciencias Médicas de Holguín. Hospital General Dr. “Gustavo Aldereguía Lima”. Holguín, Cuba.
2Universidad de Ciencias Médicas de Holguín. Hospital General Universitario “Vladimir Ilich Lenin”. Holguín, Cuba.
*Autor para la correspondencia. Correo electrónico: yoandernap@gmail.com
RESUMEN
Introducción: La fibrilación auricular paroxística es una arritmia con alta tasa de recurrencia tras la ablación por catéter. La identificación de factores predictivos es crucial para estratificar el riesgo y guiar estrategias de seguimiento orientadas a reducir el impacto funcional y las potenciales complicaciones asociadas.
Objetivo: Identificar factores predictivos de recurrencia de fibrilación auricular paroxística tras la ablación por catéter.
Métodos: Se realizó una revisión sistemática en PubMed, Cochrane, LILACS y SciElo (2014-2024). Para la estrategia de búsqueda se emplearon operadores booleanos; se revisaron estudios originales en inglés, portugués y español que admitieran adultos sometidos a ablación por catéter, y que identificaran factores clínicos, electrocardiográficos y ecocardiográficos predictores de recurrencia postablación. Se excluyeron preprints y artículos que no incluyeran seres humanos. De los 313 registros identificados, 9 cumplieron los criterios de inclusión.
Resultados: Se involucraron a 4219 pacientes con fibrilación auricular paroxística. Las recurrencias se observaron en 1403 casos (33,25 %). Los predictores clínicos relevantes identificados fueron: Tratamiento hemodialítico, positividad de la prueba de la mesa basculante, consumo de alcohol y frecuencia cardiaca en reposo < 50 latidos/min. Entre los predictores electrocardiográficos destacaron: Índice de bajo voltaje auricular y bloqueo interauricular avanzado. Los predictores ecocardiográficos destacados constituyeron: Diámetro de aurícula izquierda y regurgitación mitral funcional.
Conclusiones: La recurrencia de la fibrilación auricular paroxística tras la ablación por catéter se asocia con un perfil multifactorial de riesgo y predominan los factores predictivos que se relacionan con la conducción eléctrica y el crecimiento de cavidades.
Palabras clave: ablación por catéter; ecocardiografía; electrocardiografía; factores de riesgo; fibrilación auricular; revisión sistemática.
ABSTRACT
Introduction: Paroxysmal atrial fibrillation is an arrhythmia with high recurrence rate after catheter ablation. The identification of predictive factors is essential for risk stratification and guiding follow-up strategies aimed at reducing functional impairment and potential associated complications.
Objective: To identify predictive factors for recurrent paroxysmal atrial fibrillation after catheter ablation.
Methods: A systematic review was conducted on PubMed, Cochrane, LILACS, and SciELO databases (2014–2024). Boolean operators were used in the search strategy. Original studies in English, Portuguese, and Spanish involving adult patients after catheter ablation, and which identified clinical, electrocardiographic, and echocardiographic predictors of recurrence were included. Preprints and studies not involving human participants were excluded. Of the 313 records identified, 9 were included.
Results: A total of 4,219 patients that suffer from paroxysmal atrial fibrillation were involved. Recurrences were reported in 1,403 patients (33.25%). Relevant clinical predictors included hemodialysis treatment, head-up tilt test positive, alcohol consumption and resting heart rate < 50 beats/min. Electrocardiographic predictors included low voltage index and interatrial advanced block. Relevant echocardiographic predictors included left atrial diameter and functional mitral regurgitation.
Conclusions: Recurrence of paroxysmal atrial fibrillation after catheter ablation is associated with a multifactorial risk profile, and predictive factors related to electrical conduction and chamber growth predominate.
Keywords: atrial fibrillation; catheter ablation; echocardiography; electrocardiography; risk factors; systematic review.
Recibido: 09/06/2025
Aprobado: 28/02/2026
INTRODUCCIÓN
La fibrilación auricular (FA) se considera la arritmia cardiaca más frecuente.(1) Dicho elemento justifica el calificativo de enfermedad epidémica global del siglo XXI.(2) La fibrilación auricular paroxística (FAP) representa una forma clínica con temporalidad particular, definida por Van Gelder IC y otros(3) como episodios de “FA que terminan antes de 7 días, de forma espontánea o con asistencia de una intervención”.
La prevalencia estimada en 1998 era de 1 – 2 % en mayores de 65 años y progresaba a FA permanente en aproximadamente 20 % de los casos.(4) El 25 % de los pacientes con diagnóstico de FA y el 55,6 % de los casos sintomáticos presentan un patrón paroxístico.(5,6) En Italia se estimó una prevalencia de 449 000 pacientes mayores de 65 años durante 2016, mientras que en Europa la proyección fue de 3 185 000 en igual periodo.(7) En Japón, el registro RAFFINE detalla que el 37,8 % de los 3 901 participantes tenían FAP.(8)
En Cuba, Sariol-González PA y otros(9) plantean que de 2020 a 2021 se egresaron del Hospital Clínico Quirúrgico “Celia Sánchez Manduley” 85 pacientes con diagnóstico de FAP. Regal VM y otros(10) informan que entre 2020 y 2022 se hospitalizaron en el Servicio de Cardiología del Hospital “Dr. Gustavo Aldereguía” 54 pacientes con primer evento de FA. En la provincia Holguín, Rondón-Vázquez AF y otros(11) determinan que 46 % de los pacientes que asistían a la consulta de FA del Hospital “Vladimir Lenin” durante el año 2017 presentaban recurrencias de la arritmia. Mayo MA(12) recopila que 31 (29,81 %) de los pacientes atendidos en el servicio de Medicina Interna del Hospital Clínico-Quirúrgico “Lucía Íñiguez” durante el año 2022, presentaron FAP.
Los datos alertan sobre un problema de salud emergente, en el que estratificación del riesgo de recurrencia de FAP es vital para guiar estrategias de seguimiento orientadas a reducir el impacto funcional y las potenciales complicaciones asociadas.
El objetivo de esta revisión es identificar factores predictivos de recurrencia de fibrilación auricular paroxística tras la ablación por catéter.
MÉTODOS
Protocolo
Se siguieron las recomendaciones del Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA 2020) para revisiones sistemáticas y se registró en el International Prospective Register of Systematic Reviews (PROSPERO) con ID: CRD420251019711, actualizado 02/01/2026.(13,14) Las modificaciones posteriores consistieron en refinar el título y objetivo. Se recopilaron datos de investigaciones publicadas y no se requirió aprobación por Comités de Ética Médica institucionales.
Estrategia de búsqueda
Se accedió a PubMed, Cochrane, LILACS y SciElo para rastrear estudios publicados entre 2014-2024. El día 19/12/2025 se realizó la última búsqueda actualizada en idioma inglés, portugués y español. Los términos y operadores booleanos empleados se recogen en el material adicional.
Las referencias obtenidas fueron importadas a Zotero 7.0.15 y se eliminaron duplicados. Nápoles-Zaldivar y Nodarse-Palacios, con mediación de Silva-Velasco; revisaron cada título y resumen de forma manual e independiente. De los estudios que pasaron a la última fase, se revisó el texto completo. El diagrama de flujo fue construido según recomendaciones PRISMA 2020.
Selección de artículos
Se utilizaron como criterios de inclusión:
Pacientes adultos (≥ 19 años) con diagnóstico de FAP, independiente del tiempo de evolución o el número de episodios previos. Todos los pacientes fueron sometidos a un procedimiento de ablación por catéter (por radiofrecuencia o crioablación).
Estudios que evaluaran la asociación entre recurrencia de FAP y factores predictivos documentados en registros médicos con análisis univariado o multivariado. Estos se clasificaron por categorías:
Clínicos: Edad, sexo, índice de masa corporal (IMC), hábitos tóxicos (alcoholismo, tabaquismo), comorbilidades (hipertensión arterial, diabetes mellitus, apnea obstructiva del sueño, enfermedad cardíaca estructural), tratamiento hemodialítico, duración de la FA.
Electrocardiográficos: Parámetros derivados del trazado de 12 derivaciones en ritmo sinusal, estudios electrofisiológicos o Holter (duración/amplitud de onda P, bloqueo interauricular, índice de bajo voltaje, frecuencia cardíaca en reposo).
Ecocardiográficos: Parámetros morfológicos y funcionales (diámetro, área, volumen de aurícula izquierda), valvulopatías, fracción de eyección ventricular izquierda.
Se excluyeron los artículos de tipo preprints y aquellos que no involucraron estudios en humanos.
Evaluación de sesgo
Los estudios observacionales se evaluaron con Risk of Bias in Non-randomized Studies of Interventions (ROBINS-IV2).(15) Los datos fueron procesados en Robvis, programado en R.(16) A su vez, 2 revisores (Nápoles-Zaldivar y Nodarse-Palacios) evaluaron el riesgo de sesgo y en caso de conflictos, Silva-Velasco tomó la decisión final.
Extracción de datos
Se recopilaron datos por 2 revisores de forma independiente: Estudio, año, país, diseño, intervención, muestra, FAP recurrente, definición de grupos, factor predictivo, valor de corte (cuando se reflejara en los artículos), razón de riesgos (hazard ratio)(HR), p-valor y seguimiento.
Síntesis de resultados
Para simplificar la información se construyeron tablas donde se distribuyeron por cada estudio, los factores predictivos, con su correspondiente HR, intervalo de confianza y p-valor. Las estimaciones ajustadas se priorizaron y cuando no estuvieron disponibles, se utilizaron estimaciones crudas. Se consideraron significativos los factores con p ≤ 0,05. Los datos se redondearon a 2 decimales.
RESULTADOS
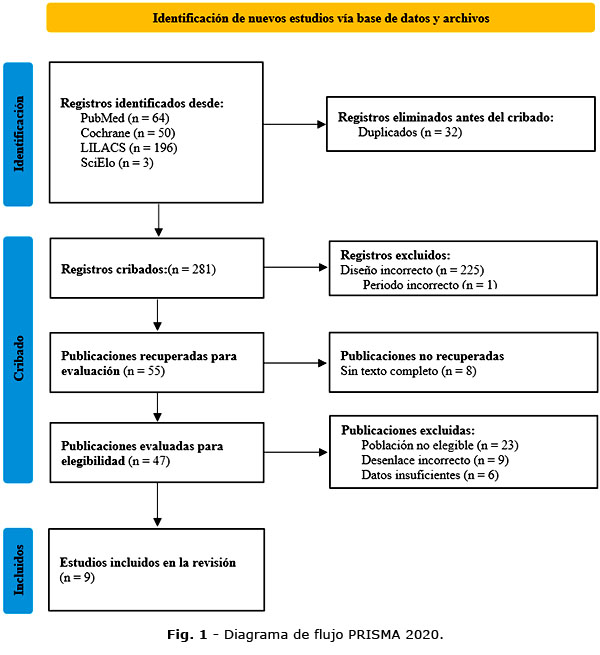
Se identificaron 313 artículos. Luego de eliminar duplicados, revisión de títulos, resúmenes y textos completos, se incluyeron 9 estudios (Fig. 1). Todos eran observacionales de cohorte (4 prospectivos, 5 retrospectivos). En conjunto, se analizaron 4219 pacientes con FAP sometidos a ablación. Se reportó recurrencia en 1403 (33,25 %) pacientes. En la tabla 1 se resume las características de los estudios.
Predictores postablación
El mayor riesgo de recurrencia de FAP se asoció con la hemodiálisis, la positividad de la prueba de la mesa basculante, el consumo de alcohol y la frecuencia cardiaca en reposo < 50 latidos/min. Dentro de los predictores electrocardiográficos, el índice de bajo voltaje y el bloqueo interauricular avanzado fueron los más destacados. El diámetro de aurícula izquierda (DAI) y la regurgitación mitral funcional (RMF) encabezaron los principales factores predictivos ecocardiográficos. En la tabla 2 se perfilan los predictores identificados.
La evaluación del riesgo de sesgo se muestra en la figura 2. Llama la atención que los dominios más problemáticos fueron: Sesgo por datos perdidos (3 estudios con riesgo alto) y por selección de resultados reportados (2 estudios con riesgo alto). Tres estudios se clasificaron con riesgo de sesgo general serio.
DISCUSIÓN
Durante la ejecución de la revisión, no se identificaron estudios incluibles en pacientes tratados con cardioversión. Dicho hallazgo metodológico es crítico y determinó un refinamiento en el título y objetivo, al ser imposible abordar el objetivo comparativo inicial (predictores en cardioversión vs. ablación). Esta brecha en la literatura es clínicamente relevante, al dejar sin herramientas validadas para estratificación de riesgo a pacientes que; por limitaciones de acceso o contraindicación, sean manejados con cardioversión como terapia definitiva. La identificación de predictores en este contexto es un área de investigación urgente.
Entre los predictores clínicos, se encuentra la hemodiálisis (HD). Las modificaciones del equilibrio electrolítico pueden precipitar episodios intra y peridiálisis de FA, y con más de 6 minutos de duración, triplica el riesgo de hospitalización.(26) Desde otro punto de vista, el entorno proarrítmico generado en pacientes con enfermedad renal crónica (ERC) sometidos a HD, se relaciona con sobrecarga de volumen crónica y del sistema renina-angiotensina-aldosterona (RAAS).(27,28)
Takigawa M y otros(17) enfatizan que en la población hemodializada, el número de fármacos antiarrítmicos fallidos es un predictor independiente de recurrencia y confiere un peor pronóstico en el mantenimiento del ritmo sinusal post-procedimiento. Esto sugiere que la ablación temprana puede ser una estrategia más efectiva.
La positividad de la prueba de la mesa basculante evidencia disfunción barorrefleja y se asocia con mayor vulnerabilidad a la recurrencia de la FAP.(18) Este hallazgo coincide con lo reportado por Ferreira M y otros(29) en 68 pacientes con FAP “lone” (sin signos de enfermedad cardiovascular). Por otra parte, Zuk A y otros(30) observan que la crioablación produce una disminución significativa y aguda de la sensibilidad barorrefleja, pero no evalua la correlación entre cambios agudos y el riesgo de recurrencia a largo plazo. Kondo H y otros(31) señalan que la ausencia de reducción de la sensibilidad barorrefleja postablación puede indicar una ablación insuficiente y mayor riesgo de recurrencia.
El alcohol tiene un efecto proarrítmico.(32) Se asocia a reducción de la refractariedad a nivel auricular, enlentece la velocidad de conducción e incrementa la actividad ectópica auricular.(33) Brunner S y otros(34) sintetizan que durante el periodo en que el paciente bebe (1 - 5 horas) y el periodo de recuperación (6 - 19 h) ocurre un incremento de arritmias auriculares (incluyendo FA). En igual medida, el consumo crónico favorece el remodelado estructural, el estrés neurohormonal y los desórdenes cardiometabólicos.(35)
La frecuencia cardiaca en reposo (< 50 latidos/min) puede reflejar disfunción del nodo sinusal, hipertonía vagal y remodelado eléctrico auricular, que favorecen la actividad auricular ectópica sostenida. El HR encontrado refuerza su utilidad como marcador de vulnerabilidad eléctrica auricular, más que como signo de protección cardiovascular. Morseth B y otros(36) asocian una FC < 50 latidos/min con mayor incidencia de FA en los 20 484 participantes, seguidos durante 23 años del estudio Tromsø. El metaanálisis(37) del consorcio AFGen (n=38 981) confirma una asociación en forma de curva en “U”, con incremento del riesgo tanto en frecuencias bajas como altas.
Con alusión a predictores electrocardiográficos, el área de bajo voltaje auricular y su normalización a través de un índice, se sitúa como uno de los predictores más robustos de recurrencia de FAP tras ablación. Starek Z y otros(38) abordan que un área > 28 % de la AI con voltaje < 0,5 mV presenta un HR significativamente superior para recurrencia de FA [HR (IC 95 %): 4,82 (2,08–11,18); p< 0,01]. Su superioridad predictiva radica en la capacidad para cuantificar el sustrato arrítmico fibrótico, lo cual puede redefinir en un futuro la forma en que se identifican subgrupos de alto riesgo. Por otra parte, las Guías EHRA/HRS/APHRS/LAHRS 2024(39) sobre ablación de FA también lo reconocen como marcador de predictor de recurrencia.
El bloqueo interauricular, representa un bloqueo completo del haz de Bachmann con desincronía de la actividad auricular, lo cual actúa como trigger para el mantenimiento de arritmias.(40) Intzes S y otros(41) asocian la duración de onda P (DOP) al riesgo de recurrencias de FA: > 120 ms [OR (IC 95 %): 2,04 (1,16–3,58); p < 0,01] vs. > 150 ms [OR (IC 95 %): 10,89 (4,53–26,15); p < 0,01]. A su vez, Kreimer F y otros(42) al evaluar a 366 pacientes con antecedentes de enfermedad cerebrovascular criptogénica sometidos a monitorización cardiaca detallan que la DOP duplica el riesgo de FA.
El diámetro de aurícula izquierda (DAI) es el predictor más reportado y con mayor consistencia. Su relación con la FAP se establece en dependencia del grado de remodelado estructural, al promover fibrosis, alteraciones en la conducción eléctrica y aumento de la presión intrauricular.(43) Iglesias O y otros(44) durante su investigación sobre la influencia del remodelado estructural en las recurrencias de FA, detallan que los pacientes con dilatación de AI tienen un riesgo moderado de recurrencias. En relación con lo anterior, Yaman B y otros(45) aportan hallazgos sólidos de que los pacientes con diámetro superior a 44 mm presentan un riesgo mayor de FA postcardioversión.
La regurgitación mitral funcional figura como predictor ecocardiográfico de remodelado auricular avanzado y de sustrato eléctrico desfavorable.(21) Su traducción electro-anatómica es la dilatación y disfunción auricular izquierda con pérdida del acoplamiento atrio‑ventricular, lo que perpetúa cambios estructurales y eléctricos que sostienen la arritmia.(46) Gertz ZM y otros(47) concluyen que se relaciona con mayor recurrencia de FA tras la ablación, aunque su impacto está mediado por el tamaño de la AI. El subanálisis del ensayo CABANA aporta información que correlaciona la presencia de regurgitación mitral con un aumento del 46 % del riesgo de recurrencia de FA tras ablación, atribuible al remodelado auricular.(48)
Otros factores importantes a considerar
Los investigadores consideran que la mayor duración de FAP (años desde el diagnóstico hasta la ablación; diagnosis-to-ablation time, DAT) se asocia con mayor riesgo de recurrencias postablación, con evidencias que apoyan el beneficio de la ablación temprana (especialmente dentro de 1 año).(49) Chew DS y otros(50) encuentran en su meta-análisis que incluyó 4950 pacientes que el DAT ≤ 1 año se asocia con menor recurrencia vs. >1 año [RR (IC 95 %): 0,73 (0,65–0,82); p < 0,01].
El índice volumétrico de aurícula izquierda (IVAI) se asocia a episodios de FAP recurrente postablación y post-cardioversión.(19,51) Su determinación precisa el grado de remodelado estructural y funcional auricular y traduce sobrecarga hemodinámica crónica, como consecuencia del aumento en la presión de llenado del ventrículo izquierdo.(46) La disfunción diastólica avanzada conduce a activación sostenida de vías profibróticas y estrés oxidativo, que promueven un microambiente proarrítmico, facilita las recurrencias, perpetúa eventos paroxísticos y se asocia a mayor recurrencia al 1 año.(39,52)
Los autores reconocen como limitaciones el sesgo de selección al limitar la búsqueda a PubMed, Cochrane, LILACS y SciElo. La revisión no pudo cumplir con el objetivo inicial de incluir pacientes tratados con cardioversión. Por lo tanto, los hallazgos pueden no ser generalizables a la población con FAP no intervenida. Se recomienda tener en cuenta la heterogeneidad potencial entre estudios al emplear diferentes técnicas de ablación, las definiciones variables de recurrencia y duraciones desiguales del seguimiento,
Se concluye que la recurrencia de FAP tras ablación por catéter se asocia con un perfil multifactorial de riesgo. Este hallazgo resalta la importancia de una evaluación pre-ablación integral para identificar a los pacientes que se beneficiarían de estrategias de ablación más extensas o de un seguimiento más intensivo.
REFERENCIAS BIBLIOGRÁFICAS
1. Leal Balón E. Fibrilación auricular. En: Vicente Peña E. Medicina Interna. Diagnóstico y Tratamiento. [Internet]. 3.a ed. La Habana: Ciencias Médicas; 2022. p. 240-9. [acceso: 26/03/2025]. Disponible en: http://www.bvscuba.sld.cu/libro/medicina-interna-diagnostico-y-tratamiento-3ra-ed/
2. Kornej J, Börschel CS, Benjamin EJ, Schnabel RB. Epidemiology of Atrial Fibrillation in the 21st Century: Novel Methods and New Insights [Internet]. Circ Res. 2020; 127(1):4-20. DOI: 10.1161/CIRCRESAHA.120.316340
3. Van Gelder IC, Rienstra M, Bunting KV, Casado-Arroyo R, Caso V, Crijns HJGM, et al. 2024 ESC Guidelines for the management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS) [Internet]. Eur Heart J. 2024; 45(36):3314-414. DOI: 10.1093/eurheartj/ehae176
4. Guédon-Moreau L, Kouakam C, Kacet S. Epidemiology of paroxysmal auricular fibrillation [Internet]. Arch Mal Coeur Vaiss. 1998 [acceso: 01/04/2025]; 91(1):67–71. Disponible en: https://pubmed.ncbi.nlm.nih.gov/9749266/
5. Zoni-Berisso M, Lercari F, Carazza T, Domenicucci S. Epidemiology of atrial fibrillation: European perspective [Internet]. Clin Epidemiol. 2014; 6:213-20. DOI: 10.2147/CLEP.S47385
6. Krisai P, Blum S, Aeschbacher S, Beer J, Moschovitis G, Witassek F, et al. Associations of symptoms and quality of life with outcomes in patients with atrial fibrillation [Internet]. Heart. 2020; 106(23):1847–52. DOI: 10.1136/heartjnl-2019-316314
7. Di Carlo A, Zaninelli A, Mori F, Consoli D, Bellino L, Balderesch M. Prevalence of Atrial Fibrillation Subtypes in Italy and Projections to 2060 for Italy and Europe [Internet]. J Am Geriatr Soc. 2020; 68(11):2534–41. DOI: 10.1111/jgs.16748
8. Miyazaki S, Miyauchi K, Hayashi H, Tanaka R, Nojiri S, Miyazaki T, et al. Registry of Japanese patients with atrial fibrillation focused on anticoagulant therapy in the new era: The RAFFINE registry study design and baseline characteristics [Internet]. J Cardiol. 2018; 71(6):590–6. DOI: 10.1016/j.jjcc.2017.10.021
9. Sariol-González PA, de la Rosa-Santana JD, Verdecia-Acuña F, Meriño-Pompa Y, Naranjo-Vázquez SY. Caracterización clínica-epidemiológica de pacientes egresados con fibrilación auricular paroxística [Internet]. Rev Ciencias Médicas. 2024 [acceso: 01/04/2025]; 28(2024):e6418. Disponible en: http://revcmpinar.sld.cu/index.php/publicaciones/article/view/6418
10. Regal Cuesta VM, de la Cruz Avilés LE, Hernández Cardoso AM, Valladares Carvajal F de J, Calvo Díaz LMCD, León Regal ML. Caracterización clínico-epidemiológica de pacientes con un primer evento de fibrilación auricular [Internet]. Revista Finlay. 2024 [acceso: 27/03/2025]; 14(1):14. Disponible en: https://revfinlay.sld.cu/index.php/finlay/article/view/1355
11. Rondón-Vázquez A, Riverón-Carralero W, Peña-Carballosa A, Góngora-Gómez O, Aguilera-Mastrapa M. Relación entre el remodelado estructural y el riesgo elevado de recurrencia en la fibrilación auricular [Internet]. Univ Méd Pinareña. 2020 [acceso: 28/03/2025]; 16(1):e381. Disponible en: http://www.revgaleno.sld.cu/index.php/ump/article/view/381
12. Mayo Córdova MA. Aspectos clínicos, epidemiológicos y manejo de la fibrilación auricular en el servicio de Medicina Interna [Internet]. [Tesis de Especialidad]. Holguín, Cuba: Hospital Clínico-Quirúrgico Lucía Íñiguez Landín; 2024. [acceso: 26/03/2025]. Disponible en: https://tesis.hlg.sld.cu/downloads/3694/tesisfinal%20F%208%20de%20abril.2024.pdf
13. Page M, McKenzie J, Bossuyt P, Boutron I, Hoffann T, Mulrow C, et al. Declaración PRISMA 2020: una guía actualizada para la publicación de revisiones sistemáticas [Internet]. Rev Esp Cardiol. 2021; 74(9):790-9. DOI: 10.1016/j.recesp.2021.06.016
14. Napoles-Zaldivar Y, Nodarse-Palacios IM. Predictive factors for recurrent paroxysmal atrial fibrillation[Internet]. PROSPERO. 2025 [acceso: 02/01/2026]. Disponible en: https://www.crd.york.ac.uk/PROSPERO/view/CRD420251019711
15. ROBINS-I V2 tool [Internet]. Risk of bias tools; 2022. [acceso: 23/12/2025]. Disponible en: https://www.riskofbias.info/welcome/robins-i-v2
16. McGuinness L, Higgins J. Risk‐of‐bias VISualization (robvis): An R package and Shiny web app for visualizing risk‐of‐bias assessments [Internet]. Res Synth Methods. 2021; 12(1):55-61. DOI: 10.1002/jrsm.1411
17. Takigawa M, Kuwahara T, Takahashi A, Kobori A, Takahashi Y, Okubo K, et al. The impact of haemodialysis on the outcomes of catheter ablation in patients with paroxysmal atrial fibrillation [Internet]. Europace. 2014; 16(3):327-34. DOI: 10.1093/europace/eut230
18. Xu J, Yang L, Zhang Q, Li S, Qiao Z, Fang Y, et al. Head-Up Tilt [Internet]. Int Heart J. 2015; 56(5):500-4. DOI: 10.1536/ihj.15-039
19. Evranos B, KocyigitKM D, Gurses KM, Yalcin MU, Sahiner ML, Kaya EB, et al. Increased left atrial pressure predicts recurrence following successful cryoablation for atrial fibrillation with second-generation cryoballoon [Internet]. J Interv Card Electrophysiol Int J Arrhythm Pacing. 2016; 46(2):145-51. DOI: 10.1007/s10840-016-0107-8
20. Kanzaki Y, Inden Y, Ando M, Kamikubo Y, Ito T, Mizutani Y, et al. An ECG Index of P-Wave Force Predicts the Recurrence of Atrial Fibrillation after Pulmonary Vein Isolation [Internet]. Pacing Clin Electrophysiol. 2016; 39(11):1191-7. DOI: 10.1111/pace.12956
21. Qiao Y, Wu L, Hou B, Sun W, Zheng L, Ding L, et al. Functional mitral regurgitation: predictor for atrial substrate remodeling and poor ablation outcome in paroxysmal atrial fibrillation [Internet]. Med Baltim. 2016; 95(30):e4333-e4333. DOI: 10.1097/MD.0000000000004333
22. Takigawa M, Takahashi A, Kuwahara T, Takahashi Y, Okubo K, Nakashima E, et al. Impact of Alcohol Consumption on the Outcome of Catheter Ablation in Patients With Paroxysmal Atrial Fibrillation [Internet]. J Am Heart Assoc [Internet]. 2016 [acceso: 23/12/2025]; 5(12):e004149 Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5210418
23. Motoc A, Abugattas J-P, Roosens B, Scheirlynck E, Heyndrickx B, de Asmundis C, et al. Left atrium remodeling predicts late recurrence of paroxysmal atrial fibrillation after second generation cryoballoon ablation [Internet]. Cardiovasc Ultrasound. 2018; 16(1):19-19. DOI: 10.1186/s12947-018-0137-8
24. Wu J, Fan X, Yang H, Yan L, Xu X, Duan H, et al. Usefulness of a Low Resting Heart Rate to Predict Recurrence of Atrial Fibrillation After Catheter Ablation in People ≥65 Years of Age [Internet]. Am J Cardiol. 2018; 122(1):97-101. DOI: 10.1016/j.amjcard.2018.03.025
25. Li B, Ma H, Guo H, Liu P, Wu Y, Fan L, et al. Pulmonary vein parameters are similar or better predictors than left atrial diameter for paroxysmal atrial fibrillation after cryoablation [Internet]. Braz J Med Biol Res Rev Bras Pesqui Medicas E Biol. 2019; 52(9):e8446. DOI: 10.1590/1414-431X20198446
26. Koplan BA, Winkelmayer WC, Costea AI, Roy-Chaudhury P, Tumlin JA, Kher V, et al. Implantable Loop Recorder Monitoring and the Incidence of Previously Unrecognized Atrial Fibrillation in Patients on Hemodialysis [Internet]. Kidney Int Rep. 2022; 7(2):189–99. DOI: 10.1016/j.ekir.2021.10.001
27. Law MM, Tan S-J, Wong MCG, Toussaint ND. Atrial Fibrillation in Kidney Failure: Challenges in Risk Assessment and Anticoagulation Management [Internet]. Kidney Med. 2023; 5(9):100690. DOI: 10.1016/j.xkme.2023.100690
28. Sidhu B, Mavilakandy A, Hull KL, Koev I, Vali Z, Burton JO, et al. Atrial Fibrillation and Chronic Kidney Disease: Aetiology and Management [Internet]. Rev Cardiovasc Med. 2024; 25(4):143. DOI: 10.31083/j.rcm2504143
29. Ferreira M, Laranjo S, Cunha P, Geraldes V, Oliveira M, Rocha I. Orthostatic Stress and Baroreflex Sensitivity: A Window into Autonomic Dysfunction in Lone Paroxysmal Atrial Fibrillation [Internet]. J Clin Med. 2023; 12(18):5857. DOI: 10.3390/jcm12185857
30. Zuk A, Piotrowski R, Sikorska A, Kowalik I, Kulakowski P, Baran J. Variability of baroreceptor reflex assessed by tilt table test in a patient undergoing pulmonary vein isolation [Internet]. J Interv Card Electrophysiol Int J Arrhythm Pacing. 2025; 68(2):315-23. DOI: 10.1007/s10840-023-01690-x
31. Kondo H, Shinohara T, Fukui A, Miyoshi M, Ishii Y, Otsubo T, et al. Possible Role of Baroreflex Sensitivity in Patients With Paroxysmal Atrial Fibrillation [Internet]. JACC Clin Electrophysiol. 2019; 5(4):523-5. DOI: 10.1016/j.jacep.2019.01.009
32. Alvarado JD, Zuniga P, Stringer I, Ramirez A, Cortes E, Solano J. Holiday Heart Syndrome: A Literature Review [Internet]. Cureus. 2025; 17(2):e79816. DOI: 10.7759/cureus.79816
33. Linz B, Hertel JN, Jespersen T, Linz D. Mechanisms and Therapeutic Opportunities in Atrial Fibrillation in Relationship to Alcohol Use and Abuse [Internet]. Can J Cardiol. 2022; 38(9):1352-63. DOI: 10.1016/j.cjca.2022.04.009
34. Brunner S, Krewitz C, Winter R, von Falkenhausen AS, Kern A, Brunner D, et al. Acute alcohol consumption and arrhythmias in young adults: the MunichBREW II study [Internet]. Eur Heart J. 2024; 45(46):4938-49. DOI: 10.1093/eurheartj/ehae695
35. Hatley M, Lam T, Ekeruo I, Taegtmeyer H. Alcohol and Atrial Fibrillation: An Update and New Perspectives [Internet]. Am J Med. Elsevier. 2024; 137(11):1042-8. DOI: 10.1016/j.amjmed.2024.06.038
36. Morseth B, Graff-Iversen S, Jacobsen BK, Jørgensen L, Nyrnes A, Thelle DS, et al. Physical activity, resting heart rate, and atrial fibrillation: the Tromsø Study [Internet]. Eur Heart J. 2016; 37(29):2307-13. DOI: 10.1093/eurheartj/ehw059
37. Siland JE, Geelhoed B, Roselli C, Wang B, Lin HJ, Weiss S, et al. Resting heart rate and incident atrial fibrillation: A stratified Mendelian randomization in the AFGen consortium [Internet]. PLOS ONE. 2022; 17(5):e0268768. DOI: 10.1371/journal.pone.0268768
38. Starek Z, Di Cori A, Betts TR, Clerici G, Gras D, Lyan E, et al. Baseline left atrial low-voltage area predicts recurrence after pulmonary vein isolation: WAVE-MAP AF results [Internet]. Europace. 2023; 25(9):194. DOI: 10.1093/europace/euad194
39. Tzeis S, Gerstenfeld EP, Kalman J, Saad EB, Shamloo AS, Andrade JG, et al. 2024 European Heart Rhythm Association/Heart Rhythm Society/Asia Pacific Heart Rhythm Society/Latin American Heart Rhythm Society expert consensus statement on catheter and surgical ablation of atrial fibrillation [Internet]. Heart Rhythm. 2024; 21(9):e31-149. DOI: 10.1016/j.hrthm.2024.03.017
40. Bejarano-Arosemena R, Martínez-Sellés M. Interatrial Block, Bayés Syndrome, Left Atrial Enlargement, and Atrial Failure [Internet]. J Clin Med. 2023; 12(23):7331. DOI: 10.3390/jcm12237331
41. Intzes S, Zagoridis K, Symeonidou M, Spanoudakis E, Arya A, Dinov B, et al. P-wave duration and atrial fibrillation recurrence after catheter ablation: a systematic review and meta-analysis [Internet]. Eur Eur Pacing Arrhythm Card Electrophysiol J Work Groups Card Pacing Arrhythm Card Cell Electrophysiol Eur Soc Cardiol. 2023; 25(2):450-9. DOI: 10.1093/europace/euac210
42. Kreimer F, Aweimer A, Pflaumbaum A, Mügge A, Gotzmann M. Impact of P-wave indices in prediction of atrial fibrillation-Insight from loop recorder analysis [Internet]. Ann Noninvasive Electrocardiol Off J Int Soc Holter Noninvasive Electrocardiol Inc. 2021; 26(5):e12854. DOI: 10.1111/anec.12854
43. Liu H, Chen L, Song Y, Xu Y, Zhang C. Evaluation of Left Atrial Function in Patients with Paroxysmal Atrial Fibrillation Using Left Atrial Automatic Myocardial Functional Imaging Ultrasonography [Internet]. Cardiol Res Pract. 2023; 2023:6924570. DOI: 10.1155/2023/6924570
44. Iglesias Pérez O, Cuello Bermúdez EJ, Hechavarria Martinez A, Ramón Jorge M. Remodelado estructural y riesgo de recurrencia en la fibrilación auricular[Internet]. Multimed. 1997, Centro Provincial de Información de Ciencias Médicas; 2019 [acceso: 27/03/2025]; 23(3):490-509. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_abstract&pid=S1028-48182019000300490&lng=es&nrm=iso&tlng=es
45. Yaman B, Cerit L, Günsel HK, Cerit Z, Usalp S, Yüksek Ü, et al. Is there any Link Between Vitamin D and Recurrence of Atrial Fibrillation after Cardioversion? [Internet]. Braz J Cardiovasc Surg. 2020; 35(2):191-7. DOI: 10.21470/1678-9741-2019-0166
46. Joglar JA, Chung MK, Armbruster AL, Benjamin EJ, Chyou JY, Cronin EM, et al. 2023 ACC/AHA/ACCP/HRS Guideline for the Diagnosis and Management of Atrial Fibrillation: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines [Internet]. Circulation. 2024; 149(1):e1-e156. DOI: 10.1161/CIR.0000000000001193
47. Gertz ZM, Raina A, Mountantonakis SE, Zado ES, Callans DJ, Marchlinski FE, et al. The impact of mitral regurgitation on patients undergoing catheter ablation of atrial fibrillation [Internet]. Eur Eur Pacing Arrhythm Card Electrophysiol J Work Groups Card Pacing Arrhythm Card Cell Electrophysiol Eur Soc Cardiol. 2011; 13(8):1127-32. DOI: 10.1093/europace/eur098
48. Dhont S, Bertrand PB, Erzeel J, Deferm S, Pison L, Vandervoort PM, et al. The interaction between atrial fibrillation and mitral regurgitation: Insights from the CABANA randomized clinical trial [Internet]. Eur J Heart Fail. 2025; 27(8):1500-7. DOI: 10.1002/ejhf.3668
49. Karakasis P, Tzeis S, Pamporis K, Schuermans A, Theofilis P, Milaras N, et al. Impact of catheter ablation timing according to duration of atrial fibrillation history on arrhythmia recurrences and clinical outcomes: a meta-analysis [Internet]. Europace. 2025; 27(6):euaf110. DOI: 10.1093/europace/euaf110
50. Chew DS, Black-Maier E, Loring Z, Noseworthy PA, Packer DL, Exner DV, et al. Diagnosis-to-Ablation Time and Recurrence of Atrial Fibrillation Following Catheter Ablation: A Systematic Review and Meta-Analysis of Observational Studies [Internet]. Circ Arrhythm Electrophysiol. 2020; 13(4):e008128. DOI: 10.1161/CIRCEP.119.008128
51. Águila-Gordo D, Jiménez-Díaz J, Negreira-Caamaño M, Martínez-Del Rio J, Ruiz-Pastor C, Sánchez Pérez I, et al. Usefulness of risk scores and predictors of atrial fibrillation recurrence after elective electrical cardioversion [Internet]. Ann Noninvasive Electrocardiol. 2024; 29(1):e13095. DOI: 10.1111/anec.13095
52. Chollet L, Iqbal S ur R, Wittmer S, Thalmann G, Madaffari A, Kozhuharov N, et al. Impact of atrial fibrillation phenotype and left atrial volume on outcome after pulmonary vein isolation [Internet]. Europace. 2024; 26(4):euae071. DOI: 10.1093/europace/euae071
Conflictos de interés
Los autores declaran que no existen conflictos de interés.
Información financiera
No se recibió financiamiento para realizar esta revisión.
Contribución de los autores
Conceptualización: Yoander Nápoles-Zaldivar, Ivonne María Nodarse-Palacios, Edilio Silva-Velasco
Curación de datos: Yoander Nápoles-Zaldivar, Ivonne María Nodarse-Palacios, Edilio Silva-Velasco
Análisis Formal: Yoander Nápoles-Zaldivar, Ivonne María Nodarse-Palacios, Edilio Silva-Velasco
Investigación: Yoander Nápoles-Zaldivar, Ivonne María Nodarse-Palacios, Edilio Silva-Velasco
Metodología: Yoander Nápoles-Zaldivar, Edilio Silva-Velasco
Validación: Ivonne María Nodarse-Palacios
Visualización: Yoander Nápoles-Zaldivar
Redacción - Elaboración del borrador original: Yoander Nápoles-Zaldivar, Edilio Silva-Velasco
Redacción - Revisión y edición: Ivonne María Nodarse-Palacios, Edilio Silva-Velasco
Disponibilidad de datos
Archivo complementario: Estrategia de búsqueda (PDF): Disponible en: https://revmedmilitar.sld.cu/index.php/mil/libraryFiles/downloadPublic/147