Artículo de Investigación
Factores de riesgo de rigidez arterial en pacientes con diabetes tipo 2
Risk factors for arterial stiffness in patients with type 2 diabetes
Jorge Manuel Gallego Galano1* https://orcid.org/0009-0008-2253-8967
Elio Zaldívar Alvarez1 https://orcid.org/0000-0002-2252-4994
Rafael Alberto Hernández Morales1 https://orcid.org/0009-0004-9138-1466
Víctor Samuel Ramírez Barayobre1 https://orcid.org/0000-0003-2937-3241
María Eugenia García Céspedes1 https://orcid.org/0000-0001-5075-831X
1Hospital General “Dr. Juan Bruno Zayas Alfonso”. Santiago de Cuba, Cuba.
*Autor para la correspondencia. Correo electrónico: jorgegallego@infomed.sld.cu
RESUMEN
Introducción: La rigidez arterial se asocia a complicaciones de la diabetes mellitus.
Objetivo: Identificar factores de riesgo de rigidez arterial en pacientes diabéticos tipo 2.
Métodos: Se realizó un estudio analítico de casos-controles. La población estudiada fueron todos los pacientes con diagnóstico de diabetes mellitus tipo 2 que acudieron a consulta de medicina interna del Hospital “Dr. Juan Bruno Zayas”, de Santiago de Cuba, durante el periodo de enero 2023 a julio 2024. El grupo de estudio quedó constituido por 219 personas, de los cuales 73 (casos) con rigidez arterial y 146 (controles) sin rigidez arterial. Se realizó para el análisis estadístico bivariado y multivariado el cálculo de odds ratio como estimador de riesgo. Se aplicó la prueba de hipótesis no paramétrica ji cuadrado de independencia con un nivel de significación p≤ 0,05.
Resultados: En el análisis multivariado se identificó como principales factores de riesgo de rigidez arterial : hipertensión arterial OR= 16,0 [5,08; 50,5]; hiperlipidemia OR= 9,6 [3,26-28,2]; edad≥ 60 años OR= 3,6 [1,3-9,9] y factores dependientes de la diabetes mellitus: tiempo de evolución mayor de 5 años OR= 5,9 [2,02-16,9]; hiperglucemia postprandial de dos horas OR= 5,8 [1,9-17,6] y HbAc1 aumentada OR= 5,4 [2,1-14,1], con una asociación estadísticamente significativa.
Conclusiones: Los factores de riesgo de rigidez arterial identificados incrementan el daño endotelial al amplificar la vulnerabilidad metabólica vascular.
Palabras clave: diabetes mellitus tipo 2; hipertensión arterial; rigidez arterial.
ABSTRACT
Introduction: Arterial stiffness is associated with complications of diabetes mellitus.
Objective: To identify risk factors for arterial stiffness in patients with type 2 diabetes.
Methods: An analytical case-control study was conducted. The study population consisted of all patients diagnosed with type 2 diabetes mellitus who attended the Internal Medicine clinic at “Dr. Juan Bruno Zayas Hospital” in Santiago de Cuba, Cuba, between January 2023 and July 2024. The study group comprised 219 individuals, of whom 73 (cases) with arterial stiffness and 146 (controls) without arterial stiffness. Odds ratios were calculated as a risk estimator for bivariate and multivariate statistical analysis. The non-parametric chi-square test of independence was applied with a significance level of p ≤ 0.05.
Results: In the multivariate analysis, the main risk factors for arterial stiffness were identified as: hypertension OR = 16.0 [5.08 - 50.5]; hyperlipidemia OR = 9.6 [3.26 - 28.2]; age ≥ 60 years OR = 3.6 [1.3 - 9.9]; and factors related to diabetes mellitus: duration of diabetes greater than five years OR = 5.9 [2.02 - 16.9]; two-hour postprandial hyperglycemia OR = 5.8 [1.9 - 17.6]; and elevated HbA1c OR = 5.4 [2.1 - 14.1], with a statistically significant association.
Conclusions: The identified risk factors for arterial stiffness increase endothelial damage by amplifying vascular metabolic vulnerability.
Keywords: arterial rigidity; hypertension; type 2 diabetes mellitus.
Recibido: 19/07/2025
Aprobado: 27/01/2026
INTRODUCCIÓN
A pesar de los avances en los sistemas de salud, la diabetes mellitus tipo 2 (DM2) persiste como un desafío global de salud pública, que afecta a millones de personas. Según datos de la Federación Internacional de Diabetes,(1) en 2024 convivían con esta enfermedad 589 millones de adultos, de entre 20 y 79 años; lo que equivale al 11,1 % de la población mundial, es decir, uno de cada nueve adultos. Las proyecciones son aún más alarmantes: para 2050 se espera un incremento del 46 %, que alcanzará cerca de 853 millones de personas, es decir, uno de cada ocho adultos. La DM2 concentra alrededor del 90 % de todos los casos de diabetes; se consolida como la forma más prevalente y de mayor impacto en la carga mundial de la enfermedad.
Cuba, con una población de 10 242 351 habitantes, en el año 2023, según el Anuario Estadístico de Salud, tuvo una prevalencia de DM2 de 69,3 x 1000 habitantes, con una mortalidad bruta de 22,3 defunciones x 100 000 habitantes. Estos datos la ubican como la octava causa de muerte en el país. En Santiago de Cuba la prevalencia de la enfermedad fue de 57,1 x 1000 habitantes, con una mortalidad bruta 27,6 x 100 000 habitantes.(2)
Las complicaciones macrovasculares elevan significativamente el riesgo de muerte prematura en personas con diabetes, mientras que las microvasculares afectan la calidad de vida, al incrementar la morbilidad y discapacidad. Ambas generan una considerable pérdida de años de vida productivos, altos costos personales y sociales.(1) El abordaje de esta enfermedad debe enfocarse en estrategias integrales, que incluyan la prevención primaria, el diagnóstico precoz y el manejo oportuno de cada etapa, para reducir estos indicadores de salud.
Actualmente se conoce que la rigidez arterial (RA) es un factor clave en la aparición de las complicaciones de la diabetes mellitus tipo 2 (DM2); se considera un marcador de daño vascular y predictor independiente de complicaciones.(3)
Los efectos de la RA son diversos y de gran impacto clínico. En el sistema macrovascular, la rigidez arterial acelera la aterosclerosis, el estrés endotelial; el incremento de la presión arterial sistólica genera una sobrecarga hemodinámica en el ventrículo izquierdo, con mayor riesgo de eventos isquémicos, como infarto de miocardio, accidente cerebrovascular o enfermedad arterial periférica.(4)
Por otro lado, en el plano microvascular, el aumento de la rigidez arterial en grandes arterias transmite una presión pulsátil elevada hacia arteriolas y capilares, genera disfunción endotelial, reduce la vasodilatación e hipoperfusión tisular. Estos mecanismos aceleran las complicaciones microvasculares, manifestadas como glomeruloesclerosis y proteinuria en los riñones, que incide de manera directa en el desarrollo y progresión de la enfermedad renal crónica. De forma análoga, favorece la aparición de retinopatía diabética y potencia el desarrollo o agravamiento de la neuropatía periférica.(5,6,7)
La rigidez arterial en personas con diabetes tipo 2 se asocia con factores de riesgo tradicionales, como la edad avanzada, el sexo, la hipertensión arterial (HTA) y la dislipidemia. Sin embargo, en los últimos años se ha puesto de relieve la necesidad de considerar nuevos factores relacionados directamente con la diabetes, entre los que destacan la hiperglucemia crónica, la resistencia insulínica, el estrés oxidativo y la inflamación persistente; así como analizar el papel que desempeña el control metabólico en la progresión del daño vascular.(3)
La RA se puede evaluar mediante la velocidad de la onda de pulso (VOP) carotídeo-femoral, utilizando la fotopletismografía digital, con el equipo ANGIODIN® PD 3000, dispositivo médico portátil, disponible en los hospitales de Santiago de Cuba, diseñados en el Centro de Biofísica Médica de esta ciudad.(8)
La razón principal que justifica la medición de la RA en la práctica clínica es la evaluación de su valor predictivo para el desarrollo de episodios cardiovasculares. Además, proporciona una información pronóstica complementaria, a la aportada por factores clásicos de riesgo cardiovascular. Comprender con mayor profundidad los mecanismos asociados a la rigidez, permitirá implementar estrategias preventivas y terapéuticas más eficaces y personalizadas, dirigidas a mejorar la salud vascular, retrasar la progresión de la rigidez arterial y reducir el riesgo de eventos adversos en esta población vulnerable.
El objetivo de esta investigación es identificar los factores de riesgo de rigidez arterial en pacientes con DM2.
MÉTODOS
Diseño
Se realizó un estudio observacional analítico, de casos y controles, en el período de enero del año 2023 a julio de 2024, en la consulta externa de medicina interna del Hospital General “Dr. Juan Bruno Zayas Alfonso”, de la provincia de Santiago de Cuba.
Sujetos
La población estudiada fueron todos los pacientes con diagnóstico de diabetes mellitus tipo 2, que acudieron a consulta en el periodo de estudio. La muestra quedó constituida por 219, con edad ≥ 30 años, que se realizaron estudios bioquímicos y de hemodinamia vascular. De ellos se seleccionaron todos los casos con rigidez arterial (n= 73) y como grupo control de la misma población, se seleccionaron los pacientes sin rigidez arterial (n= 146), mediante muestreo aleatorio simple, con una relación de 1:2.
Se excluyeron pacientes con discapacidades motoras y mentales, quienes no completaron los estudios requeridos o presentaron datos clínicos incompletos.
Variables
Variable dependiente: rigidez arterial.
Variables independientes (las que se asociaron a la aparición de rigidez arterial).
Demográficas:
Edad ≥ 60 años: Sí/No.
HTA: presión arterial ≥ 140/90 mm/Hg (Sí/No).
Obesidad abdominal: circunferencia de la cintura ≥ 102 cm en hombres y ≥ 88 cm en mujeres (Sí/No).
Hábito tabáquico: definidas según las recomendaciones de la OMS(9) (Sí/No).
Alcoholismo:(10) ingestión mayor de 1 onza de alcohol puro diario, que equivale a 1 onza (20 mL) de etanol, 8 onzas (240 mL) de vino, 24 onzas (720 mL) de cerveza, 1,5 onzas (45 mL) de ron, de acuerdo con los criterios taxonómicos para los patrones de consumo etílico (Sí/No).
Tiempo de evolución de la diabetes mellitus tipo 2: se consideró > 5 años (Sí/No).
Variabilidad glucémica: se evaluó con el perfil glucémico registrado en la historia clínica ambulatoria. Se consideró dos o más oscilaciones en los niveles de glucosa en sangre, evaluados en las última 24 h (promedio mayor de 10 mosml/L), elevaciones de glucosa en ayuno (mayor de 10 mosml/L) y episodios de hipoglucemia (menor de 3,9 mosml/L) (Sí/No).
Hiperlipidemia: se consideró 2 o más alteraciones lipídicas patológicas (colesterol total > 6,2 mmol/L, LDLc ≥ 4,1 mmol/L, HDLc < 1,3 mmol/L, triglicéridos > 1,50 mmol/L) (Sí/No).
Hiperglucemia postprandial de dos horas: se consideró los valores de glucemia a las dos horas después de las principales comidas ≥ 10 mmol/L (Sí/No).
Hemoglobina glucosilada (HbAc1): se consideró aumentada a valores > 7,0 % (Sí/No).
Microalbuminuria: se consideró excreción urinaria de albúmina entre 20 y 200 μg/min (Sí/No).
Ecodoppler carotídeo: se evaluó el grosor de la íntima media carotídea (GIM): se consideraron valores > de 1,1 mm (Sí/No).
Ecocardiograma transtorácico de reposo: se evaluó exclusivamente la presencia de hipertrofia del ventrículo izquierdo concéntrica o excéntrica. Se definió mediante el índice de la masa ventricular izquierda (IMVI) y el grosor relativo de la pared (GRP). Se consideró hipertrofia cuando el IMVI fue > 115 g/m² en hombres, o > 95 g/m² en mujeres. El GRP se clasificó como normal si < 0,42 y patológico si ≥ 0,42. Con estos criterios, la hipertrofia se tipificó como concéntrica (IMVI elevado y GRP ≥ 0,42, con cavidad normal y paredes engrosadas) o excéntrica (IMVI elevado y GRP < 0,42, con cavidad dilatada y paredes engrosadas)(11) (Sí/No).
Rigidez arterial aumentada: se determinó mediante fotopletismografía, realizada con el pletismógrafo digital ANGIODIN® PD 3000 (2020). Se consideraron patológicos, valores de la velocidad de la onda de pulso carotídeo-femoral (PWV) ≥ 2,51 a 10 m/s (Sí/No).
Procesamiento estadístico
Se realizó con IBM-SPSS v. 22 para Windows. Se confeccionó una base de datos con Microsoft Excel. Para el análisis bivariado se aplicaron pruebas de ji cuadrado para evaluar la independencia entre las variables categóricas y la presencia de rigidez arterial. Se consideraron significativas las asociaciones con valores de p< 0,05. Se calculó el odds ratio (OR) y sus intervalos de confianza. Se consideró su nivel de confianza (IC) del 95 %.
Se consideraron como factores de riesgo las variables con OR> 1. Fueron significativas las que el límite inferior del IC del OR para el 95 %, estuviese por encima de 1. Después se realizó regresión logística, para determinar cuáles variables mantienen asociación significativa con la rigidez arterial, con ajuste por covariables y evaluar el riesgo probabilístico con las variables seleccionadas. Finalmente, se evaluó la calibración del modelo a través de la prueba de bondad de ajuste de Hormer-Lemeshow, con un nivel de significación de 0,05 para decidir su utilidad; valores p> 0,05 indicaron un ajuste adecuado del modelo.
Aspectos bioéticos
El estudio se rigió por los criterios éticos en concordancia con la política institucional y los principios de la Declaración de Helsisnki.(11) Se aprobó por el Comité de Ética Médica y el Consejo Científico de la institución hospitalaria. Todos los participantes en la investigación mostraron su conformidad mediante la firma del consentimiento informado.
RESULTADOS
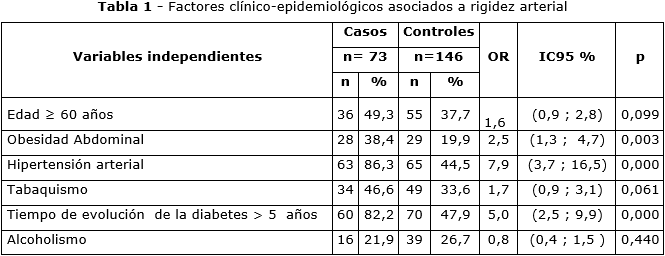
El análisis estadístico bivariado (tabla 1) mostró que la HTA fue el factor de riesgo más frecuente OR= 7,9 [IC95 %: 3,7-16,5 ], al incrementar 8 veces la probabilidad de presentar RA si está presente el factor. Además, otros factores con significación estadística fueron: tiempo de evolución de la diabetes mayor de 5 años OR= 5,0 [IC95 %: 2,5-9,9] y la obesidad abdominal OR= 2,5 [IC95 %: 1,3-4,72]. Sin embargo, resultó llamativo que variables como la edad ≥ 60 años, el tabaquismo y el alcoholismo, no mostraron asociación estadísticamente significativa con el riesgo de desarrollar RA.
En el análisis de los factores humorales (tabla 2), la hemoglobina glucosilada (HbAc1) resultó el predictor más relevante, con OR= 7,9 [IC95 %: 4,2-14,9]; un paciente con este factor tiene 8 veces más probabilidad de tener RA, en relación con quien no presenta este factor. Asimismo, los parámetros vinculados al control metabólico mostraron asociaciones significativas: la hiperlipidemia con OR= 6,6 [IC95 %: 3,2-13,6] y la hiperglucemia postprandial con un OR= 3,9 [IC95 %: 1,9-7,8], lo cual confirmó que el descontrol glucémico y lipídico potencializó el daño vascular. Finalmente, la microalbuminuria también se relacionó con mayor riesgo de RA, con OR= 2,1 [IC95 %: 1,1-4,1], lo que reflejó un daño renal incipiente, estrechamente vinculado a la progresión del daño vascular.
En relación con los estudios imagenológicos (tabla 3); la hipertrofia ventricular izquierda mostró asociación significativa, OR= 2,1 [IC95 %: 1,2-3,7]; el paciente con este factor tiene 2 veces más probabilidad de presentar RA, que quienes no presentan el factor. Además, la consolida como un marcador del riesgo cardiovascular. En contraste, el GIM no evidenció asociación significativa; no aportó capacidad discriminativa en esta población.
En el análisis multivariado (tabla 4) se identificaron como predictores independientes de RA, la HTA, con OR= 16,0 [IC95 %: 5,08–50,5; p< 0,001] y la hiperlipidemia con OR= 9,6 [IC95 %: 3,26–28,2; p< 0,001]; ambos con la mayor asociación, seguidos por el tiempo de evolución de la diabetes mayor de 5 años OR= 5,9 [IC95 %: 2,02–16,9; p< 0,001], la hiperglucemia postprandial de dos horas, OR= 5,8 [IC95 %: 1,9–17,6; p< 0,001] y la HbA1c aumentada OR= 5,4 [IC95 %: 2,1–14,1; p< 0,001]. Reflejaron el impacto, tanto del control glucémico agudo como crónico en el daño vascular. La edad ≥ 60 años, OR= 3,6 [IC95 %: 1,3–9,9; p= 0,01] y la obesidad abdominal OR= 3,6 [IC95 %: 1,2–10,6; p= 0,02] mostraron asociaciones significativas de menor magnitud y confirmaron que la RA resultó de la interacción de factores hemodinámicos, metabólicos y clínicos, que al interactuar simultáneamente potencializaron el riesgo cardiovascular.
La prueba de Hosmer–Lemeshow (χ²= 8,033; p= 0,430) indicó que el modelo de regresión logística presentó buen ajuste; que no hubo diferencias significativas entre lo predicho y lo observado; las estimaciones fueron válidas y consistentes.
DISCUSIÓN
Los resultados muestran asociación significativa entre la RA aumentada, con factores de riesgo individuales, como HTA, hiperlipidemia, edad ≥ 60 años y obesidad abdominal, asociados a factores dependientes de la DM2 como el tiempo de evolución > 5 años, la presencia de hiperglucemia postprandial de dos horas y la HbAc1. Estas variables, reconocidas como componentes de riesgo cardiovascular, mostraron efectos aditivos y estadísticamente significativos sobre la RA, lo cual sugiere un papel sinérgico en la progresión del daño arterial estructural. Estos hallazgos confirman que la RA resulta de la convergencia entre factores clásicos de riesgo cardiovascular y parámetros de deficiente control metabólico; configura un perfil de gran relevancia clínica.
Por otra parte, la hipertensión arterial resulta el mejor predictor, al aumentar 16 veces la probabilidad de presentar RA; mientras que el tiempo de evolución mayor de 5 años mantiene vigencia como el marcador metabólico más robusto, al incrementar más de 5 veces el riesgo. Estos resultados en conjunto subrayan la necesidad de un abordaje integral, que priorice tanto el control de la HTA, como el metabólico, para reducir de manera efectiva la carga de daño vascular en esta población.
Staef M y otros,(13) encontraron asociación de la RA con la edad (β= 0,405; p< 0,001), la presión arterial sistólica (β= 0,421; p< 0,001) y el tiempo de evolución de la diabetes (β= 0,073; p= 0,038), lo que coincide con esta investigación. Sin embargo, refuerza lo expuesto por otros autores,(3,14) que demuestran que la RA no constituye un hallazgo colateral, sino un marcador dinámico de riesgo cardiovascular y resaltan la necesidad de su determinación para prevenir eventos cardiovasculares. Se ha demostrado que en pacientes con DM2, la HTA se relaciona estrechamente con la RA, en un proceso bidireccional. En la DM2, la hiperglucemia crónica y la resistencia a la insulina favorecen la glicación avanzada, reducen la elasticidad arterial y aumentan la velocidad de la onda de pulso, lo que contribuye al desarrollo de HTA(15) y a su vez, la HTA agrava la RA mediante el estrés hemodinámico crónico y el remodelado vascular, lo cual consolida un círculo vicioso, que acelera el daño cardiovascular.(16,17)
Lo expuesto confirma lo encontrado por Tian X y otros(18) en un estudio de cohorte, de más de 11 000 personas, en China, con una media de seguimiento de 6,16 años. Demostraron que la diabetes se asocia, no solo con la HTA, sino también con la RA; lo cual muestra mayor capacidad que la HTA sola para predecir la diabetes. Por otra parte, Nikolaidou B y otros,(19) en Grecia, al igual que González D y otros,(20) en España, demostraron la asociación de la RA con la HTA, LDLc y DM2.
Otro factor identificado fue la hiperlipidemia, que mostró asociación estadísticamente significativa, OR= 5,5 [2,60-11,83] y clínicamente relevante con la RA; lo que indica que un paciente con DM2, que presente este factor, tiene un riesgo 5 veces mayor de presentar RA, en relación con quien no lo presente. Este hallazgo coincide con estudios previos, que atribuyen este vínculo a mecanismos como la disfunción endotelial, estrés oxidativo, aterogénesis y pérdida de la elasticidad arterial, con mayor riesgo de eventos cardiovasculares agudos.(21,22)
Gottsäter M y otros(23) evidenciaron que los marcadores de riesgo y predictores de RA a largo plazo son: la edad (β=0,38; p< 0,001), obesidad abdominal (β= 0,17; p< 0,001), hiperglucemia (β= 0,13; p< 0,001), niveles elevados de triglicéridos (β= 0,10; p< 0,001) y bajo nivel de colesterol HDL (β= −0,08, p< 0,001), luego de ajustar la presión arterial media y la frecuencia cardíaca como factor de riesgo. Esto coincide con los hallazgos de Liang YQ y otros,(24) en el estudio longitudinal Riesgo de aterosclerosis en comunidades (ARIC), en cuatro comunidades de EE. UU.
Un hallazgo relevante se observó al analizar el papel de la edad ≥ 60 años, la cual, en el análisis bivariado solo mostró una tendencia hacia un mayor riesgo de RA (OR= 1,6; IC95 %: 0,9–2,8; p= 0,099), sin alcanzar significación estadística. Se puede explicar por fenómenos de colinealidad y confusión con otros factores de riesgo, así como por limitaciones de poder estadístico. Sin embargo, en el modelo multivariado, tras ajustar por covariables, como HTA, hiperlipidemia, control glucémico y obesidad abdominal, la edad fue un predictor independiente y significativo (OR= 3,6; IC95 %: 1,3–9,9; p= 0,01).
En consecuencia, la edad ≥ 60 años se confirmó como un factor de riesgo, con asociación independiente de RA, en pacientes con DM2, lo cual se sustenta en una base fisiopatológica que explica cómo el envejecimiento vascular, en combinación con un entorno metabólico adverso, incluso en ausencia de otros factores de riesgo, acelera el deterioro estructural y funcional de las arterias.(25)
En el estudio longitudinal Evolución de la RA y su relación con factores de riesgo cardiovascular (EVA)(26) realizado en España durante cinco años, se encontró en el análisis de regresión múltiple, que la edad mostró una asociación significativa con el aumento de todos los parámetros de RA, OR= 3,12 [2,01-4,85]. De igual forma, otras variables como dislipidemia, OR= 1,78 [1,12-2,84] y DM2, OR= 2,45 [1,35-4,45] mostraron asociación significativa, aunque de menor magnitud. Estos resultados refuerzan lo encontrado en la investigación y en estudios realizados por Vasan RS y otros,(27) que demuestra una vez más que el envejecimiento vascular no solo refleja el paso del tiempo, sino que actúa como determinante fisiopatológico clave en la progresión de la RA, con un impacto significativo en poblaciones de alto riesgo.
En relación con los factores dependientes de la diabetes, la duración de la enfermedad superior a cinco años se ha identificado como un factor de riesgo significativo para el desarrollo de RA en pacientes con DM2, que integra la carga acumulada de agresión metabólica y vascular. No obstante, diversos estudios han demostrado que la RA puede estar presente, ya al momento del diagnóstico, lo cual refleja daño vascular subclínico, acumulado por la exposición previa a HTA, hiperlipidemia, obesidad y otros factores de riesgo.(3,13,28) Sin embargo, la hiperglucemia postprandial de dos horas, al reflejar picos de perjudiciales, y la HbAc1 crónica sostenida, son indicadores útiles del control glucémico, que contribuyen a la disfunción endotelial, el estrés oxidativo, al estado inflamatorio crónico, con formación de productos finales de glicación avanzada, que modifican la estructura del colágeno, la elastina y producen endurecimiento de la pared arterial.(29) Así, mientras la rigidez arterial puede ser incipiente y reversible en fases iniciales, tras los cinco años de evolución, se consolida como un marcador persistente y clínicamente relevante de daño cardiovascular.
Shibib L y otros,(30) en una revisión, muestran que la hiperglucemia postprandial en el paciente diabético es un marcador fuerte e independiente de aterogénesis, de complicaciones macrovasculares y microvasculares, con mayor riesgo de mortalidad cardiovascular; además, presenta un valor predictivo mayor que la glucosa en ayunas y HbAc1.(31) Sin embargo, el valor relativo de dichas variables (glucemia en ayunas frente a glucemia postprandial y la HbAc1) es poco comprendido o aplicado por los profesionales sanitarios, lo que conlleva a peores resultados para los pacientes.
Una fortaleza del presente estudio radica en la identificación de los factores de riesgo relacionados con la aparición de RA, en pacientes con DM2; evidencia que la RA no debe ser solo un dato más; es un marcador clave, que puede facilitar el diseño de estrategias terapéuticas personalizadas, más eficaces, en la prevención y el tratamiento de enfermedades cardiovasculares. Entre las limitaciones se encuentra el carácter monocéntrico, tamaño muestral limitado, en un periodo de tiempo corto; que limitan la generalización de los resultados a poblaciones más amplias.
Se concluye que la HTA, la hiperlipidemia, la edad ≥ 60 años, la obesidad abdominal en presencia de factores dependientes de la DM2 como: tiempo de evolución > 5 años, la presencia de hiperglucemia postprandial de dos horas y la HbAc1 elevada, son los factores de riesgo identificados en la aparición de RA en el paciente diabético tipo 2.
REFERENCIAS BIBLIOGRÁFICAS
1. International Diabetes Federation. IDF Diabetes Atlas, 11º Edición [Internet]. Bruselas, Bélgica: International Diabetes Federation; 2025. [acceso: 07/06/2025]. Disponible en: https://diabetesatlas.org
2. Oficina Nacional de Estadística e Información. Anuario Estadístico de Cuba [Internet]. La Habana: ONEI; 2024. [acceso: 07/06/2025]. Disponible en: http://files.sld.cu/dne/files/2024/09/Anuario-Estad%c3%adstico-de-Salud-2023-EDICION-2024.pdf
3. Gallego J, Pérez Y, Álvarez RA, García ME, Bell J. Rigidez arterial en la evaluación del riesgo cardiovascular en el diagnóstico de la diabetes tipo 2 [Internet]. Rev. card. cir. Cardiovasc. 2025 [acceso: 07/06/2025]; 31: e_2255. Disponible en: https://revcardiologia.sld.cu/artcle/view/2255
4. Wu Z, Yu S, Zhang H, Guo Z, Zheng Y, Xu Z, et al. Combined evaluation of arterial stiffness, glycemic control and hypertension for macrovascular complications in type 2 diabetes [Internet]. Cardiovasc Diabetol. 2022; 21(1): 262. DOI: 10.1186/s12933-022-01696-1
5. Brady RP, Urbina EM, Gao Z, Dabelea D, Lustigova E, Marcovina S, et al. Arterial stiffness is related to microvascular complications associated with diabetes: the SEARCH for Diabetes in Youth study [Internet]. Diabetes Care. 2025;48(4):639-647. DOI:10.2337/dc24-2320
6. Partalidou S, Patoulias D, Pantekidis I, Kefas A, Doumas M, Gkaliagkousi E, et al. The cross-talk between arterial stiffness and microvascular complications in diabetes mellitus: a systematic review of the literature [Internet]. J Diabetes Metab Disord. 2025;24(2):144. DOI: 10.1007/s40200-025-01647-z
7. Beros A, Sluyter J, Scragg RKR. Association of arterial stiffness and neuropathy in diabetes: a systematic review and meta-analysis [Internet]. BMJ Open Diabetes Research & Care. 2023; 11: e003140. DOI:10.1136/bmjdrc-2022-003140
8. García-Céspedes M, Copello M, Pascau A, Bell J, Romero F. Rigidez arterial como marcador de daño vascular en pacientes con hipertensión arterial controlada [Internet]. MEDISAN. 2018 [acceso: 08/06/2025]; 22(9): 931. Disponible en: http://scielo.sld.cu/scielo.php?pid=S1029-30192018000900931&script=sci_arttext
9. World Health Organization. WHO report on the global tobacco epidemic, 2025: warning about the dangers of tobacco [Internet]. Geneva: World Health Organization; 2025. [acceso: 30/11/2025]. Disponible en: https://www.who.int/publications/i/item/9789240112063
10. González R. Un criterio taxonómico para los patrones de consumo etílico [Internet]. Rev. Cub. Salud Púb. 2011 [acceso: 30/11/2025]; 37(1): 132-43. Disponible: https://www.redalyc.org/articulo.oa?id=21417788011
11. Lang RM, Badano LP, Mor-Avi V, Afilalo J, Armstrong A, Ernande L, et al. Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging [Internet]. J Am Soc Echocardiogr. 2015;28(1): 1-39.e14. DOI:10.1016/j.echo.2014.10.003
12. World Medical Association. Declaration of Helsinki: ethical principles for medical research involving human subjects [Internet]. JAMA. 2013 [acceso: 08/06/2025]; 310(20):2191-4. Disponible en: https://jamanetwork.com/journals/jama/fullarticle/1760318
13. Staef M, Ott C, Kannenkeril D, Striepe K, Schiffer M, Schmieder E, et al. Determinantes de la rigidez arterial en pacientes con diabetes mellitus tipo 2: un análisis transversal [Internet]. Sci Rep. 2023; 13(1): 8944. DOI: 10.1038/s41598-023-35589-4
14. Vallée A. Arterial Stiffness Determinants for Primary Cardiovascular Prevention among Healthy Participants [Internet]. J Clin Med. 2022;11(9):2512. DOI:10.3390/jcm1109251
15. Ahmadizar F, Wang K, Roos M, Bos M, Mattace F, Kavousi M. Association between arterial stiffness/remodeling and new-onset type 2 diabetes mellitus in general population [Internet]. Diabetes Res Clin Pract. 2023; 196:110237. DOI: 10.1016/j.diabres.2023.110237
16. Díaz C, Patiño AJ, Rosales LY, Loredo I, Martínez E, González M. Índice de rigidez arterial ambulatorio en pacientes diabéticos [Internet]. Rev Med Chile. 2020 [acceso: 06/12/2025]; 148(4):496-503. Disponible en: https://www.scielo.cl/scielo.php?pid=S0034-98872020000400496&script=sci_arttext&tlng=pt
17. Galvão RDV, Pereira CS, Freitas EGB, Lima DRART, Santos WAM, Souza DF, Nomelini QSS, Ferreira-Filho SR, et al. Association between diabetes mellitus and central arterial stiffness in elderly patients with systemic arterial hypertension [Internet]. Clin Exp Hypertens. 2020; 42(8):728-32. DOI: 10.1080/10641963.2020.1783547
18. Tian X, Zuo Y, Chen S, Zhang Y, Zhang X, Xu Q, et al. Hypertension, Arterial Stiffness, and Diabetes: a Prospective Cohort Study [Internet]. Hypertension. 2022; 79(7):1487-96. DOI: 10.1161/HYPERTENSIONAHA.122.19256
19. Nikolaidou B, Anyfanti P, Lazaridis A, Nashoufidou A, Malliora A, Kordalis V, et al. Type 2 diabetes mellitus: an independent factor in increased carotid stiffness [Internet]. Journal of Hypertension. 2025; 43(1):127. DOI:10.1097/01.hjh.0001116448.45597.e6
20. Gonzáles Falcón D, Gómez Sánchez L, Gómez Sánchez M, Rodríguez E, Tamayo O, Lugones C, et al. Evolución de la rigidez arterial y asociación con factores de riesgo cardiovascular en población española. Seguimiento del estudio EVA [Internet]. Med Clin (Barc). 2025; 164(9): 461-9. DOI: 10.1016/j.medcli.2024.11.008
21. Quilligana SA, Cevallos AC. Dislipidemias e hipertensión en pacientes con Diabetes Mellitus II [Internet]. MQRInvestigar. 2024 [acceso: 08/06/2025]; 8(1):168–85. Disponible en: https://www.investigarmqr.com/ojs/index.php/mqr/article/view/883
22. Baba M, Maris M, Jianu D, Luca CT, Stoian D, Mozos I. The Impact of the Blood Lipids Levels on Arterial Stiffness [Internet]. J Cardiovasc Dev Dis. 2023;10(3):127. DOI: 10.3390/jcdd10030127
23. Gottsäter M, Östling G, Persson M, Engström G, Melander O, Nilsson PM. Predictores no hemodinámicos de rigidez arterial después de 17 años de seguimiento: el estudio Malmö Diet and Cancer [Internet]. J Hipertensión. 2015; 33(5): 957–65. DOI:10.1097/HJH.0000000000000520
24. Liang YQ, Zhou R, Chen HW, Cao BF, Dong FW, Liu K, et al. Asociaciones de biomarcadores sanguíneos con la rigidez arterial en pacientes con diabetes mellitus: Un estudio poblacional [Internet]. J Diabetes. 2023 [acceso: 07/06/2025]; 15(10):853-65. Disponible en: https://pubmed.ncbi.nlm.nih.gov/37329140/
25. Li A, Yan J, Zhao Y, Yu Z, Tian S, Khan AH, et al. Vascular Aging: Assessment and Intervention [Internet]. Clinical interventions in aging. 2023 [acceso: 07/06/2025]; 18:1373-1395. Disponible en: https://pubmed.ncbi.nlm.nih.gov/37609042/
26. Gómez M, Patino MC, Gómez L, Recio JI, Rodríguez E, Maderuelo JA, et al. Valores de referencia de parámetros de rigidez arterial y su relación con los factores de riesgo cardiovascular en población española. Estudio EVA [Internet]. Rev Esp Cardiol. 2020 [acceso: 07/06/2025]; 73(1): 43-52. Disponible en: https://www.revespcardiol.org/es-valores-referencia-parametros-rigidez-arterial-articulo-S0300893219301654
27. Vasan RS, Pan S, Xanthakis V, Beiser A, Larson MG, Seshadri S, et al. Arterial Stiffness and Long-Term Risk of Health Outcomes: The Framingham Heart Study [Internet]. Hypertension. 2022 [acceso: 07/06/2025];79(5):1045-56. Disponible en: https://pubmed.ncbi.nlm.nih.gov/35168368/
28. Zheng M, Zhang X, Chen S, Song Y, Zhao Q, Gao X, et al. Arterial Stiffness Preceding Diabetes: A Longitudinal Study [Internet]. Circ Res. 2020;127(12):1491-8. DOI: 10.1161/CIRCRESAHA.120.317950
29. Pinés PJ, Bellido V, Ampudia FJ. Update on postprandial hyperglycaemia: the pathophysiology, prevalence, consequences and implications of treating diabetes [Internet]. Rev Clin Esp (Barc). 2020; 220(1): 57-68. DOI:10.1016/j.rce.2018.06.015
30. Shibib L, Al-Qaisi M, Guess N, Miras AD, Greenwald SE, Pelling M, et al. Manipulation of Post-Prandial Hyperglycaemia in Type 2 Diabetes: An Update for Practitioners [Internet]. Diabetes Metab Syndr Obes. 2024 [acceso: 07/06/2025]; 17: 3111-30. Disponible en: https://pubmed.ncbi.nlm.nih.gov/39206417/
31. Hershon KS, Hirsch BR, Odugbesan O. Importance of Postprandial Glucose in Relation to A1C and Cardiovascular Disease [Internet]. Clin Diabetes. 2019;37(3):250-9. DOI: 10.2337/cd18-0040
Conflictos de interés
Los autores no declaran conflictos de interés.
Información financiera
Los autores no recibieron financiamiento para la realización de este trabajo.
Contribuciones de los autores
Conceptualización: Jorge Manuel Gallego Galano, Víctor Samuel Ramírez Barayobre, María Eugenia García Céspedes, Rafael Alberto Hernández Morales.
Análisis formal: Elio Zaldívar Alvarez, Jorge Manuel Gallego Galano.
Investigación: Jorge Manuel Gallego Galano, Elio Zaldívar, Víctor Samuel Ramírez Barayobre, Rafael Alberto Hernández Morales.
Metodología: Elio Zaldívar Alvarez, Jorge Manuel Gallego Galano, Víctor Samuel Ramírez Barayobre.
Supervisión: Jorge Manuel Gallego Galano, María Eugenia García Céspedes.
Validación: Elio Zaldívar Alvarez, Jorge Manuel Gallego Galano, María Eugenia García Céspedes.
Administración del proyecto: Jorge Manuel Gallego Galano.
Redacción - Elaboración del borrador original: Víctor Samuel Ramírez Barayobre, Rafael Alberto Hernández Morales, Jorge Manuel Gallego Galano.
Redacción-Revisión y edición: Jorge Manuel Gallego Galano, Elio Zaldivar Alvarez, María Eugenia García Céspedes.
Disponibilidad de datos
Archivo complementario: Base de datos de investigación (Excel). Disponible en: https://revmedmilitar.sld.cu/index.php/mil/libraryFiles/downloadPublic/139