Artículo de Investigación
Perfil de radiodensidades en lesiones pulmonares residuales de COVID-19
Radio density profile in residual lung lesions of COVID-19
Ángel René Elejalde Larrinaga1 https://orcid.org/0000-0003-2356-5365
Natascha Mezquia de Pedro2 https://orcid.org/0000-0002-7859-3841
Consuelo Milagro Macías Abraham3 https://orcid.org/0000-0001-5484-096X
Danay Corrales Otero4 https://orcid.org/0000-0002-1522-2357
Claudia Elejalde Tamayo1 https://orcid.org/0000-0002-4148-0448
Evelio Gonzalez Dalmau5* https://orcid.org/0000-0003-4569-2103
1Instituto de Oncología y Radiobiología (INOR). Departamento de Consulta Externa de Neumología La Habana, Cuba.
2Universidad de Ciencias Médicas de La Habana. Facultad de Ciencias Médicas “Dr. Miguel Enríquez”. La Habana, Cuba.
3Instituto de Hematología e Inmunología. Departamento de Investigaciones. La Habana, Cuba.
4Instituto de Oncología y Radiobiología (INOR). Departamento de Imagenología. La Habana, Cuba.
4Centro de Neurociencias de Cuba (CNEURO). Departamento de Imágenes. La Habana, Cuba.
*Autor para la correspondencia. Correo electrónico: evelio.gonzalez@cneuro.edu.cu
RESUMEN
Introducción: La tomografía computarizada (TC) es crucial para evaluar las secuelas pulmonares post-COVID-19. Sin embargo, la caracterización de las lesiones residuales se basa predominantemente en descripciones cualitativas, por tanto, existe una brecha en la cuantificación objetiva de su densidad.
Objetivo: Identificar los perfiles de radiodensidad en unidades Hounsfield (UH) de las lesiones pulmonares residuales en pacientes post-COVID-19.
Métodos: Estudio transversal, en 26 pacientes con secuelas pulmonares por la COVID-19. Se analizaron imágenes de TC de alta resolución (TCAR), se definieron regiones de interés (ROI) en patrones de imagen específicos. La medición de la radiodensidad (UH) se realizó con la herramienta ROI del software eFilm. El análisis estadístico incluyó ANOVA para comparar los perfiles.
Resultados: Se identificaron y cuantificaron cuatro patrones radiológicos con perfiles de radiodensidad distintos y significativamente diferentes (p< 0,0001): 1) Tejido sano: -900 a -800 UH; 2) patrón indefinido: -799 a -701 UH; 3) opacidad en vidrio deslustrado (OVD): -700 a -500 UH; 4) consolidación pulmonar (CP): -499 a -201 UH. Se estableció un punto de corte en -500 UH para diferenciar la OVD de la CP. El patrón indefinido representa un hallazgo novedoso.
Conclusión: Se proponen por primera vez rangos cuantitativos específicos de UH para las lesiones pulmonares post-COVID-19. Definir estos perfiles, incluido un "patrón indefinido", proporciona una herramienta objetiva y estandarizable para el diagnóstico, caracterización y seguimiento de la enfermedad pulmonar intersticial post-COVID-19. Sienta las bases para aplicarla en la práctica clínica y la investigación futura.
Palabras clave: COVID-19; enfermedades pulmonares intersticiales; lesión pulmonar; pulmón; tomografía computarizada por rayos X.
ABSTRACT
Introduction: Computed tomography (CT) is crucial for evaluating pulmonary sequelae in post-COVID-19 patients. However, residual lesion characterization relies predominantly on qualitative descriptions, lacking objective density quantification.
Objective: To quantify radiodensity profiles in Hounsfield Units (HU) of residual lung lesions in post-COVID-19 patients.
Methods: Cross-sectional study of 26 patients with post-COVID-19 pulmonary sequelae. High-resolution CT (HRCT) images were analyzed by defining regions of interest (ROI) on specific imaging patterns. Radiodensity (HU) was measured using eFilm software's ROI tool. Statistical analysis included ANOVA for profile comparisons.
Results: Four distinct radiological patterns with significantly different radiodensity profiles were identified (p < 0.0001): 1) Healthy tissue: -900 to -800 HU; 2) Undefined pattern: -799 to -701 HU; 3) Ground-glass opacity (GGO): -700 to -500 HU; 4) Pulmonary consolidation (PC): -499 to -201 HU. A -500 HU cutoff differentiated GGO from PC. The undefined pattern represents a novel finding.
Conclusion: This study proposes the first specific quantitative HU ranges for post-COVID-19 pulmonary lesions. These radiodensity profiles provide an objective, standardized tool for diagnosing, characterizing, and monitoring post-COVID-19 interstitial lung disease, establishing foundations for clinical practice and future research.
Keywords: COVID-19; cross-sectional studies; lung; lung diseases, interstitial; lung injury; tomography, X-Ray computed.
Recibido: 29/09/2025
Aprobado: 30/04/2026
INTRODUCCIÓN
Los avances en tomografía computarizada (TC) han mejorado el diagnóstico no invasivo de enfermedades pulmonares, particularmente del intersticio pulmonar.(1,2) El análisis tomográfico utiliza el coeficiente de atenuación tisular, cuantificado en unidades Hounsfield (UH), en el cual el agua representa 0 UH, el aire -1000 UH y los huesos +1000 UH.(3)
Los estudios radiómicos describen metodologías innovadoras para extraer datos matemáticos de imágenes médicas,(4) aunque sus aplicaciones prácticas siguen siendo limitadas.(5) En infecciones virales con daño alveolar difuso, se observan patrones característicos en TC de alta resolución, que representan alteraciones anatomopatológicas asociadas a neumonía organizada, patrones estándar en enfermedades pulmonares intersticiales difusas.(6)
Existen reportes que demuestran persistencia de imágenes en convalecientes de hasta cinco años en la influenza tipo A(7) y 15 años en SARS-CoV-1.(8) El reconocimiento de imágenes similares en convalecientes de SARS-CoV-2 sugiere que los daños iniciales causan secuelas tardías. Los sobrevivientes de la COVID-19 presentan síntomas persistentes, denominados secuelas postagudas de la COVID-19 (PASC), relacionados con la inmunidad del huésped, daño tisular y mecanismos de infección multiorgánica.(9,10,11)
A pesar de los avances en la caracterización cualitativa, existe una brecha significativa en la cuantificación objetiva de perfiles de radiodensidad de las lesiones residuales. La mayoría de estudios previos se centran en la descripción visual, sin definir rangos numéricos precisos que diferencien tejido sano, opacidades en vidrio deslustrado y consolidaciones. Esta falta de estandarización dificulta la comparación entre estudios, el seguimiento longitudinal y la evaluación de la respuesta terapéutica.
La cuantificación de daños mediante regiones de interés (ROI), con software especializado, permite la evaluación objetiva del pronóstico.(12,13) Dada la escasez de estudios que definan rangos precisos de radiodensidad para diferentes patrones de daño, resulta fundamental abordar esta brecha de conocimiento.
Este trabajo plantea como pregunta de investigación: ¿Cuál es el valor de identificar perfiles de radiodensidad en patrones imagenológicos de daños pulmonares residuales por la COVID-19? La hipótesis propone que es posible identificar perfiles específicos, que faciliten la caracterización y seguimiento de pacientes con estas lesiones.
El objetivo es identificar los perfiles de radiodensidad en unidades Hounsfield (UH) de las lesiones pulmonares residuales en pacientes post-COVID-19.
MÉTODOS
Diseño
Estudio observacional, de corte transversal, en imágenes de TCAR de tórax, en un grupo de pacientes convalecientes de la COVID-19, realizado entre los meses de abril y agosto del año 2020, en el Centro de Neurociencias de la Habana.
Sujetos
Se seleccionó una muestra intencional de 26 pacientes en quienes se identificaron lesiones pulmonares residuales de COVID en la TCAR, a partir de una serie de 54 pacientes con persistencia de síntomas respiratorios, sin antecedentes conocidos de enfermedad pulmonar, con 92 días como promedio a partir de la infección aguda, que fueron reclutados para recibir tratamientos con células madre autólogas en el Instituto de Hematología e Inmunología, de la Habana.
Variables
Edad y sexo.
Patrón de imagen: Interpretación de las imágenes de la TCAR por el observador para definir patrones de imagen relacionados con anomalías pulmonares intersticiales.
a) Normal: Se caracteriza por tejido bien aireado y distribución homogénea de vasos y bronquios en la estructura, sin opacidades ni nódulos.
b) Opacidad de vidrio deslustrado (OVD): Se presenta como un ligero aumento de la densidad pulmonar con preservación parcial de los márgenes de los vasos pulmonares y bronquios, creando áreas definidas de daño.
c) Opacidad de consolidación pulmonar (OCP): Corresponde a un aumento homogéneo de la atenuación del parénquima pulmonar, con pérdida de contornos vasculares y ocasionalmente broncograma aéreo, creando áreas bien definidas de parches.
Perfil de radiodensidades: Se expresa en valores de las medias de radiodensidad, en áreas de cortes axiales en los patrones de imágenes con representatividad, definidos por el observador y expresados UH, con diámetro entre 5 a 10 mm².
Procedimientos
En la variable patrón de imagen, otros patrones de imágenes vinculados con el incremento en la densidad pulmonar se asociaron con la gravedad de los daños, la localización y la evolución en las lesiones pulmonares.
En el perfil de radiodensidades, las imágenes se visualizaron con un ancho de ventana pulmonar que permite el reconocimiento de las anomalías pulmonares intersticiales. Se seleccionaron seis niveles para el análisis de los daños, definidos en: Unión del esternón y la clavícula, origen de la arteria innominada, borde inferior del arco aórtico, arteria pulmonar izquierda, arteria pulmonar derecha y porción inferior de la aurícula izquierda.
Para identificar el perfil se utilizó una “herramienta” de la barra de trabajo del sistema de diagnóstico eFilm, designada por una circunferencia con las siglas ROI; la “herramienta” se obtiene al hacer clic en el icono y se arrastra sobre el área de la imagen que desea medir. El diámetro se define durante la colocación manual desde el centro a la periferia, en la ROI y los datos de la media (µ) aparecen de forma automática al liberar el mouse . La media en cada ROI ser promedió para obtener el perfil de las medias de ambos pulmones.
Técnica de obtención de los datos
Las TCAR se realizaron en tomógrafo PET/CT Gemini TOF TF64, de 64 cortes, en el Instituto de Oncología y Radiobiología en La Habana, Cuba. Se empleó el protocolo de “Chest”, con inspiración máxima. Parámetros en el escáner: Voltaje del tubo a 120 kVp, modulación automática de corriente de 70 a 120 mAs y campo de reconstrucción de 350 mm. Matriz de 512 × 512 píxeles; píxel 0,68 x 0,68 mm (0,4624 mm²). Reconstrucción con algoritmo de alta resolución espacial, espesor de cortes 1 a 3 mm, uso de retroproyección filtrada y filtro estándar tipo C. Se anonimizaron las imágenes mediante el software de código abierto, DICOM Browser.
Para el control del sesgo de selección, tres profesionales con experiencia en el manejo y evaluación de imágenes tomográficas de tórax (radiólogo, neumólogo y bioingeniero), seleccionaron cinco estudios con representación de anomalías pulmonares intersticiales y se les practicó de forma exploratoria la identificación del perfil de radiodensidad en los patrones de imágenes y después en el resto de las TCAR.
Se realizaron 8 mediciones promedios por estudio.
Análisis estadístico
El análisis estadístico y gráfico se realizó con GraphPad Prism 9.5.0. Los patrones de imagen se identificaron a partir de reportes primarios; se definieron los perfiles como rangos de valores basados en la media (µ) de las unidades Hounsfield (UH). Se calculó el coeficiente de variación (CV); se aceptó para el análisis valores menores al 20 %. Tras confirmar la normalidad de la distribución mediante la prueba de Kolmogorov-Smirnov, se aplicó un ANOVA de una vía para comparar las medias entre los distintos patrones. El nivel de significación estadística se estableció en p< 0,05.
Consideraciones bioéticas
Los procedimientos de investigación se diseñaron sin interacción directa con pacientes, utilizando exclusivamente datos de estudios de TCAR. Para garantizar la confidencialidad, todos los datos identificables fueron anonimizados y enmascarados, cumpliendo con los principios éticos establecidos en la Declaración de Helsinki. gEl proyecto fue evaluado por el Comité de Ética de las investigaciones del Instituto de Hematología e Inmunología, donde radicó la investigación base.
RESULTADOS
La caracterización de los pacientes no mostró diferencias en relación con el sexo, con 15 mujeres para el 57,69 % y una edad media 56,28 años.
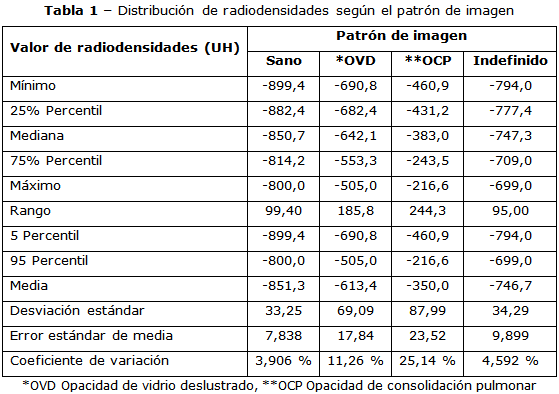
En la tabla 1 se muestra la estadística descriptiva en la distribución de las radiodensidades calculando los valores mínimos (5 percentil) y los valores máximos (95 percentil). Llama la atención la identificación de un rango de valores de radiodensidades no definidos en ninguno de los patrones propuestos inicialmente para el análisis. Los autores lo clasificaron como patrón indefinido e incluyó radiodensidades entre los valores del patrón de pulmón sano y el de OVD. El coeficiente de variación se mantuvo por debajo del 20 %, excepto en las mediciones obtenidas en la OCP, lo que indica una elevada variabilidad de los datos obtenidos en ese patrón.
En la tabla 2 se muestran los rangos de radiodensidades, según patrón de imagen, entendidos estos como perfil de radiodensidad. Se identificaron cuatro patrones de imágenes, en un rango de valores de radiodensidades que va desde -899 UH hasta -216 UH. El perfil de radiodensidad del patrón indefinido se movió en un rango de radiodensidad entre (-794 a -699 UH). Se realizó una propuesta de referencia en los perfiles de los patrones encontrados, que permite mejor manejo de los datos desde el punto de vista práctico al quedar definidos por números enteros.
En la figura 1 se observan los perfiles de radiodensidades de cada patrón, con expresión de perfil propio, sin interposición, visualmente separados, con diferencias estadísticas significativas (p< 0,0001), que confirman la individualidad de cada uno.
DISCUSIÓN
Las lesiones pulmonares residuales de la COVID-19 fueron reconocidas en las imágenes de TCAR mediante patrones de imágenes definidos. Múltiples investigadores han destacado el papel de las imágenes de alta resolución para el reconocimiento de las anomalías pulmonar intersticial.(14,15)
El diámetro promedio de las ROI fue de 7,45 mm² lo cual permitió el reconocimiento del acino pulmonar y otras estructuras del intersticio. Debido a la complejidad anatómica del lobulillo pulmonar secundario, no es posible correlacionarlo directamente con una ROI, por ello, el análisis integra múltiples áreas de distintos lobulillos. Las áreas con mayores afectaciones fueron las regiones subpleurales periféricas, los septos interlobares y los tabiques interlobulillares, con menor impacto en áreas del intersticio peribroncovascular distal al hilio.
La OVD fue el patrón de mayor representación en las lesiones pulmonares residuales, con predominio en la periferia entre los niveles en los cuales irriga la arteria innominada y el borde inferior del arco aórtico. La OCP mostró áreas de parches en regiones periféricas de segmentos y subsegmentos, y preferencia a por la porción inferior de la aurícula izquierda. La asociación de OVD y OCP se designaron como patrones típicos del daño en las lesiones residuales de la COVID-19 y también en las enfermedades pulmonares intersticiales difusas (EPID).(16,17)
El engrosamiento de los septos interlobulares se vinculó con imágenes lineales que definen daño reticular periférico y se diferenciaron de las líneas B de Kerley.(18) La combinación del patrón lineal en los septos lobulillares y OVD se denomina “crazy-paving”, típico de fases avanzadas. Además, el broncograma aéreo en áreas de condensación sugiere retracción bronquial. El patrón nodular refleja daño alveolar sectorizado, quedando incluidos dentro de las anomalías asociadas con incremento de la densidad.
Las anomalías pulmonares intersticiales se asumieron como una forma particularizada de los daños del virus en el órgano. El colapso alveolar con pérdida de función y de la arquitectura, representa el soporte histológico en los daños del patrón de OVD.(19) En tanto existió otra forma de expresión, mediada por proliferación de células inflamatorias y fibroblastos dentro del alveolo, lo cual provoca respuesta local y ensanchamiento de los septos, en reconocimiento de la neumonía organizada para el patrón de OCP. La inmunotrombosis y la angiogénesis resultaron formas de manifestar los daños en las lesiones residuales.(19,20) La ausencia de panalización constituyó el diagnóstico diferencial con la fibrosis pulmonar idiopática y deja por sentado que las lesiones residuales descritas son una forma alternativa en el diagnóstico.(21)
Las lesiones pulmonares residuales requirieron de un análisis exhaustivo y se definen como el cuerpo de la evidencia para que sean declaradas como una enfermedad pulmonar intersticial clínicamente significativa en pacientes con PASC. Resultó oportuno conceptualizarlas como lesión pulmonar residual a COVID-19 (LPRC-19). Es un tipo de EPID, con un patrón alternativo de neumonía intersticial usual, provocado por los daños del SARS-CoV2 en los pulmones, consistente en imágenes tomográficas con áreas de opacidades de vidrio deslustrado y focos de condensación pulmonar en forma de parches y un perfil de radiodensidad específico.
La identificación del perfil de densidad en la investigación, representó un modelo de enfermedad relacionado con el aumento de la densidad en la estructura pulmonar, en un rango de valores que van desde -690 hasta -216 UH, que representan la construcción del coeficiente de atenuación de las LPRC-19 durante el paso de los rayos X. Por lo tanto, los elementos representados en la ROI resultan un análisis matemático del equilibrio biológico en cada patrón y proporciona medidas cuantitativas de UH reproducibles en los daños.
Las imágenes monoenergéticas obtenidas en TC muestran un comportamiento dinámico de las UH, lo que dificulta diferenciar tejidos con atenuaciones similares. Además, los elementos estructurales del pulmón generan una curva de densidades proporcional a su composición.
Por lo tanto, a pesar de reconocer el papel que juegan los diferentes elementos en la caracterización de las UH en las imágenes tomográficas, existen demasiadas incertidumbres para tratarlos de forma aislada, y se reconoce que la mayor utilidad diagnóstica está al representar los patrones de manera unificada. Sin embargo, la TC espectral emplea energías variables, que permiten identificar la absorción que ofrece una mezcla de varios elementos, contenido en el llamado borde K (K edge) de los tejidos (carbono, hidrógeno, oxígeno, nitrógeno y fósforo), en los cuales las UH está determinada por la energía incidente.(22)
Negroni D y otros(23) en un análisis de los daños de la neumonía por SARS-CoV-2 definen el perfil de radiodensidades de la OVD en un rango de -700 a - 250 UH y clasifican la OCP en valores desde -250 hasta +250 UH. La variabilidad en la gravedad de la afectación en la estructura pulmonar durante la fase aguda, crea una condición diferente a la de esta investigación. La definición de variable, la interpretación de los hallazgos y la caracterización de los patrones de imágenes en la COVID-19, en ausencia de correlación histológica, crea inseguridad en el análisis comparativo de los datos.
Se concluyen cuatro perfiles de radiodensidades, uno de ellos no reconocido entre los patrones iniciales, por esta razón se designó como indefinido. Diversos autores han establecidos rangos amplios de radiodensidades en la caracterización de pulmón normal, en los cuales quedan incluidos los valores del patrón indefinido. Emad Y y otros(24) en un análisis cuantitativo del síndrome antisintetasa, en un paciente con neumonía intersticial, declaran un rango desde -900 hasta -501 UH para definir áreas de pulmón normalmente aireado. Negroni D y otros,(23) en el análisis de los daños agudos de la neumonía por SARS-CoV-2, también incluyen el rango del perfil indefinido dentro de las áreas de parénquima pulmonar normal.
A pesar de los reportes de diversos autores que enmarcan el perfil indefinido dentro de los rangos de pulmón sano, se debe señalar que en este rango de radiodensidades también quedan incluidas regiones intersticiales de vasos sanguíneos gruesos y de la anatomía perimediastinal. El haber establecido esa condición en el análisis creó una sectorización en los rangos que facilita la estratificación y proporciona un estándar cuantitativo en la evolución de los modelos.
La agresividad del adenocarcinoma en los nódulos pulmonares se ha podido predecir desde observaciones cuantitativas en las imágenes de OVD. Fangyi X y otros(25) señalan el adenocarcinoma in situ, en perfiles de -600 a -400 UH; el adenocarcinoma mínimamente invasivo, desde -600 hasta -200 UH y el adenocarcinoma invasivo, en valores de -200 hasta +100 UH. Es prudente especificar que los perfiles del adenocarcinoma en las etapas iniciales se superponen con los de las LPRC-19, en un análisis histológico donde ambos procesos comparten el modelo de incremento en la densidad pulmonar, además de los cambios asociados con DAD, la neumonía organizada y la angiogénesis.
Yabuuchi H y otros(26) designan el alcance de la OVD en un rango entre -760 hasta -500 UH en pacientes con neumonía instersticial usual asociada a esclerosis sistémica. Shin KE y otros(27) en estudio cuantitativo correlacionan el score visual del daño intersticial, con áreas incrementadas de atenuación pulmonar, definidas entre −700 a −200 UH, sin delimitar OVD con las OCP, como se propone en esta investigación.
Es pertinente señalar la existencia de otro modelo de expresión en la atenuación pulmonar, al otro extremo del pulmón sano, un grupo de entidades muestran disminución de las densidades, relacionada con el tipo de daño anatomopatológico. El enfisema reporta umbrales por debajo de -950 UH. Las áreas relativas de atenuación por debajo de -960 UH y -970 UH se correlacionan significativamente con referencias histológicas.(28,29)
La linfangiomiomatosis expresa densidades pulmonares con valores de UH por debajo de ‑950. A pesar de la semejanza con el enfisema, los quistes y la proliferación de células anormales exigen de otros análisis en la caracterización del daño cuantificable.(30) Todo esto crea una dinámica de análisis basada en modelos de enfermedades y patrones de daños en función de los cambios histopatológicos.
Limitaciones y futuras direcciones: El tamaño reducido de la muestra (n= 26) y su origen unicéntrico limitan la validez externa de los resultados. En futuras investigaciones se deberían correlacionar estos perfiles con datos histopatológicos y seguimiento a largo plazo, para evaluar su utilidad pronóstica. También es recomendable validar los rangos propuestos en cohortes más amplias y diversos contextos clínicos.
Se identificó un rango de densidades radiológicas que caracterizan un modelo de enfermedad intersticial. Los hallazgos ofrecen una herramienta diagnóstica potencial para diferenciar entre patrones sanos y lesiones residuales, lo que podría mejorar la precisión en el diagnóstico y seguimiento de pacientes post-COVID-19. Estos resultados tienen implicaciones en la práctica clínica, pues podrían ayudar a identificar a pacientes con mayor riesgo de complicaciones pulmonares a largo plazo.
REFERENCIAS BIBLIOGRÁFICAS
1. Cobo Tabar DZ, Souto Canteli DB, González Ocio DJ, Peña Sarnago DJM, Gandiaga Mandiola DA, Lázaro Serrano DM. NIU, diagnóstico paso a paso [Internet]. Seram. 2021 [acceso: 15/03/2024];1(1):35-42. Disponible en: https://piper.espacio-seram.com/index.php/seram/article/view/4204
2. Giménez-Palleiro A, Mazzini SP, Franquet T. El informe radiológico en patología intersticial pulmonar [Internet]. Radiología. 2022;64(3):215-26. DOI: 10.1016/j.rx.2022.01.007
3. Armiñana A, Montón-Gómez C, Puig-Chilet A, Infante-Fuenzalida T, Fontenla-Martínez C, Torres-Espallardó I, et al. Tomografía computarizada espectral y unidades Hounsfield: bases para una correcta interpretación [Internet]. An RANM. 2023;140(2):101-13. DOI: 10.32440/ar.2023.140.02.rev01
4. Upegui-Jiménez D, Espinosa Cruz MÁ, Gómez Milanés S, Alcántara Martínez MF. Radiómica: ¿qué es y en dónde estamos? [Internet]. Medicina (Bogotá). 2024;46(1):89-102. DOI: 10.56050/01205498.2379
5. Gillies RJ, Kinahan PE, Hricak H. Radiomics: Images are more than pictures, they are data. Radiology. 2016;278(2):563-77. DOI: 10.1148/radiol.2015151169
6. Kligerman SJ, Franks TJ, Galvin JR. From the radiologic pathology archives: organization and fibrosis as a response to lung injury in diffuse alveolar damage, organizing pneumonia, and acute fibrinous and organizing pneumonia [Internet]. Radiographics. 2013;33(7):1951-75. DOI: 10.1148/rg.337130057
7. Wang Q, Jiang H, Xie Y, Zhang T, Liu S, Wu S, et al. Long-term clinical prognosis of human infections with avian influenza A(H7N9) viruses in China after hospitalization [Internet]. EClinical Medicine. 2020;20:100282. DOI: 10.1016/j.eclinm.2020.100282
8. Ahmed H, Patel K, Greenwood DC, Halpin S, Lewthwaite P, Salawu A, et al. Long-term clinical outcomes in survivors of severe acute respiratory syndrome and Middle East respiratory syndrome coronavirus outbreaks after hospitalisation or ICU admission: A systematic review and meta-analysis [Internet]. J Rehabil Med. 2020;52(5):jrm00063. DOI: 10.2340/16501977-2694
9. Carfì A, Bernabei R, Landi F, Gemelli Against COVID-19 Post-Acute Care Study Group. Persistent symptoms in patients after acute COVID-19 [Internet]. JAMA. 2020;324(6):603-5. DOI: 10.1001/jama.2020.12603
10. Thaweethai T, Jolley SE, Karlson EW, Levitan EB, Levy B, McComsey GA, et al. Development of a definition of postacute sequelae of SARS-CoV-2 infection [Internet]. JAMA. 2023;329(22):1934-46. DOI: 10.1001/jama.2023.8823
11. Munipalli B, Seim L, Dawson NL, Knight D, Abu-Dabrh AM. Post-acute sequelae of COVID-19 (PASC): a meta-narrative review of pathophysiology, prevalence, and management [Internet]. SN Compr Clin Med. 2022;4(1):90. DOI: 10.1007/s42399-022-01167-4
12. Mandal S, Barnett J, Brill SE, Brown JS, Denney EK, Hare SS, et al. 'Long-COVID': a cross-sectional study of persisting symptoms, biomarker and imaging abnormalities following hospitalisation for COVID-19 [Internet]. Thorax. 2021;76(4):396-8. DOI: 10.1136/thoraxjnl-2020-215818
13. DenOtter TD, Schubert J. Hounsfield unit [Internet]. En: StatPearls. Treasure Island (FL): StatPearls Publishing; 2024. [acceso: 15/03/2024]. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK547721/
14. Hata A, Schiebler ML, Lynch DA, Hatabu H. Interstitial lung abnormalities: state of the art [Internet]. Radiology. 2021;301(1):19-34. DOI: 10.1148/radiol.2021204367
15. Raghu G, Remy-Jardin M, Myers JL, Richeldi L, Ryerson CJ, Lederer DJ, et al. Diagnosis of idiopathic pulmonary fibrosis. An official ATS/ERS/JRS/ALAT clinical practice guideline. Am J Respir Crit Care Med. 2018;198(5):e44-e68. DOI: 10.1164/rccm.201807-1255ST
16. Herrera Ortiz AF, Díaz Ordoñez JC, Motta Castaño MF, Peña Pérez FA. Patrones característicos de COVID-19 en tomografía de tórax: una revisión de la literatura [Internet]. Rev Neuronum. 2020 [acceso: 15/03/2024];6(4):350-68. Disponible en: https://eduneuro.com/revista/index.php/revistaneuronum/article/view/298
17. Solomon JJ, Heyman B, Ko JP, Condos R, Lynch DA. CT of post-acute lung complications of COVID-19 [Internet]. Radiology. 2021;301(2):E383-E395. DOI: 10.1148/radiol.2021211396
18. Webb WR. Thin-section CT of the secondary pulmonary lobule: anatomy and the image. Radiology. 2006;239(2):322-38. DOI: 10.1148/radiol.2392041968
19. Cabrales Fuentes J, Mendoza Cabalé AL, Zaldivar Acosta Y. Acercamiento imagenológico e histológico para el diagnóstico de lesiones pulmonares por SARS-CoV-2 [Internet]. Rev Fac Med UNAM. 2024;67(2):26-31. DOI: 10.22201/fm.24484865e.2024.67.2.04
20. Ackermann M, Verleden SE, Kuehnel M, Haverich A, Welte T, Laenger F, et al. Pulmonary vascular endothelialitis, thrombosis, and angiogenesis in Covid-19 [Internet]. N Engl J Med. 2020;383(2):120-8. DOI: 10.1056/NEJMoa2015432
21. Raghu G, Remy-Jardin M, Myers JL, Richeldi L, Ryerson CJ, Lederer DJ, et al. Diagnosis of idiopathic pulmonary fibrosis: an official ATS/ERS/JRS/ALAT clinical practice guideline [Internet]. Am J Respir Crit Care Med. 2018;198(5):e44-e68. DOI: 10.1164/rccm.201807-1255ST
22. Armiñana A, Montón-Gómez C, Puig-Chilet A, Infante-Fuenzalida T, Fontenla Martínez C, Torres-Espallardó I, et al. Tomografía computarizada espectral y unidades Hounsfield: bases para una correcta interpretación [Internet]. An RANM. 2023;140(2):101-13. DOI: 10.32440/ar.2023.140.02.rev01
23. Negroni D, Zagaria D, Paladini A, Falaschi Z, Arcoraci A, Barini M, et al. COVID-19 CT scan lung segmentation: how we do it [Internet]. J Digit Imaging. 2022;35(3):424-31. DOI: 10.1007/s10278-022-00593-z
24. Emad Y, Ragab Y, Abd-Elsalam M, Rasker JJ. Antisynthetase syndrome complicating the course of established case with rheumatoid arthritis: a rare and under-recognized overlapping disease [Internet]. Reumatol Clin (Engl Ed). 2020;16(5 Pt 1):419-22. DOI: 10.1016/j.reuma.2018.06.002
25. Xu F, Zhu W, Shen Y, Wang J, Xu R, Oudkerk C, et al. Radiomic-based quantitative CT analysis of pure ground-glass nodules to predict the invasiveness of lung adenocarcinoma [Internet]. Front Oncol. 2020;10:872. DOI: 10.3389/fonc.2020.00872
26. Yabuuchi H, Matsuo Y, Tsukamoto H, Horiuchi T, Sunami S, Kamitani T, et al. Evaluation of the extent of ground-glass opacity on high-resolution CT in patients with interstitial pneumonia associated with systemic sclerosis: comparison between quantitative and qualitative analysis [Internet]. Clin Radiol. 2014;69(7):758-64. DOI: 10.1016/j.crad.2014.03.008
27. Shin KE, Chung MJ, Jung MP, Choe BK, Lee KS. Quantitative computed tomographic indexes in diffuse interstitial lung disease: correlation with physiologic tests and computed tomography visual scores [Internet]. J Comput Assist Tomogr. 2011;35(2):266-71. DOI: 10.1097/RCT.0b013e31820ccf18
28. Mohamed Hoesein FA, de Hoop B, Zanen P, Gietema H, Kruitwagen CL, van Ginneken B, et al. CT-quantified emphysema in male heavy smokers: association with lung function decline [Internet]. Thorax. 2011;66(9):782-7. DOI: 10.1136/thx.2010.145995
29. Dirksen A, Piitulainen E, Parr DG, Deng C, Wencker M, Shaker SB, et al. Exploring the role of CT densitometry: a randomised study of augmentation therapy in alpha1-antitrypsin deficiency [Internet]. Eur Respir J. 2009;33(6):1345-53. DOI: 10.1183/09031936.00159408
30. Chen A, Karwoski RA, Gierada DS, Bartholmai BJ, Koo CW. Quantitative CT analysis of diffuse lung disease [Internet]. Radiographics. 2020;40(1):28-43. DOI: 10.1148/rg.2020190099
Conflictos de interés
Se declara que no existen conflictos de interés.
Información financiera
Los autores declaran que no hubo subvenciones involucradas en este trabajo.
Contribuciones de los autores
Conceptualización: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Consuelo Milagro Macías Abraham, Evelio González Dalmau.
Curación de datos: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Consuelo Milagro Macías Abraham, Evelio González Dalmau.
Análisis formal: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Consuelo Milagro Macías Abraham, Evelio González Dalmau.
Investigación: Ángel René Elejalde Larrinaga, Danay Corrales Otero, Claudia Elejalde Tamayo, Evelio González Dalmau.
Metodología: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Evelio González Dalmau.
Administración de proyecto: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Consuelo Milagro Macías Abraham, Evelio González Dalmau.
Recursos: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Evelio González Dalmau.
Software: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Evelio González Dalmau.
Supervisión: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Consuelo Milagro Macías Abraham, Evelio González Dalmau.
Validación: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Evelio González Dalmau.
Visualización: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Evelio González Dalmau.
Redacción - preparación del borrador original: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Evelio González Dalmau.
Redacción - revisión y edición: Ángel René Elejalde Larrinaga, Natascha Mezquia de Pedro, Evelio González Dalmau.
Disponibilidad de datos
Los datos generados y analizados en esta investigación se encuentran depositados en el Centro de Neurociencias (CNEURO), La Habana, Cuba. Por razones de confidencialidad y protección de la privacidad de los pacientes, el acceso a los datos no es público. Sin embargo, están disponibles previa solicitud fundamentada dirigida al Bioingeniero Evelio González Dalmau (gonzalez@cneuro.edu.cu). Todas las solicitudes serán evaluadas y sujetas a aprobación por el Comité de Ética del Instituto de Hematología e Inmunología.