Artículo de la Práctica Clínica
Determinación del momento óptimo para la medición del hematocrito postransfusional
Determining the optimal time for post-transfusion hematocrit measurement
Leydiana Trimiño Galindo1 https://orcid.org/0000-0001-5430-5203
Junior Vega Jiménez1,2* https://orcid.org/0000-0002-6801-5191
Rubén González Tabares1 https://orcid.org/0000-0002-4076-8650
Layanis Guardarrama Linares1 https://orcid.org/0000-0002-7013-4237
Lisneybi González González2 https://orcid.org/0009-0003-0734-2847
1Hospital Militar “Dr. Mario Muñoz Monroy”. Matanzas, Cuba.
2Universidad de Ciencias Médicas de Matanzas. Matanzas, Cuba.
*Autor para la correspondencia. Correo electrónico: drjrvega@gmail.com
RESUMEN
Introducción: Es tradicional medir el hematocrito entre las 6 a 24 horas después de la transfusión de concentrados de eritrocitos, pero esta práctica carece de sustento bibliográfico sólido.
Objetivo: Determinar el momento óptimo (30 min, 6 h, 24 h) para medir el hematocrito en el seguimiento postransfusional.
Método: Estudio observacional, prospectivo y longitudinal de evaluación tecnológica, realizado entre febrero y abril de 2025. Se incluyeron 67 pacientes adultos transfundidos. El hematocrito se midió a los 30 minutos, 6 y 24 horas postransfusión. El análisis estadístico incluyó la prueba de Friedman, el coeficiente de correlación intraclase (CCI) y el gráfico de Bland-Altman.
Resultados: La serie incluyó 67 pacientes (27 hombres y 40 mujeres), sin diferencias significativas en la distribución por sexo ni grupos etarios (19 a 59 años: 31,3 %; 60 a 74 años: 37,4 %; 75 años y más: 31,3 %; p= 0,321). No se encontraron diferencias significativas de los valores de hematocrito entre los tres momentos (prueba de Friedman, F= 0,363). Todos los CCI fueron superiores a 0,8, lo que indica una concordancia excelente, mayor entre las mediciones a los 30 minutos y 6 horas (CCI= 0,897). El análisis de Bland-Altman mostró una diferencia media cercana entre estos dos tiempos, sin sesgo sistemático.
Conclusión: La medición del hematocrito a los 30 minutos postransfusión es adecuada y confiable para representar el efecto de la unidad transfundida; muestra una excelente concordancia con mediciones posteriores.
Palabras clave: atención al paciente; hematocrito; reproducibilidad de resultados; transfusión de eritrocitos.
ABSTRACT
Introduction: It is traditional to measure hematocrit between 6 and 24 hours after red blood cell transfusion, but this practice lacks solid bibliographic support.
Objective: To determine the optimal time (30 min, 6 h, 24 h) to measure hematocrit in post-transfusion follow-up.
Method: A prospective, longitudinal, observational study of technological evaluation was conducted between February and April 2025. Sixty-seven adult patients who received transfusions were included. Hematocrit was measured at 30 minutes, 6 hours, and 24 hours post-transfusion. Statistical analysis included the Friedman test, the intraclass correlation coefficient (ICC), and the Bland-Altman plot.
Results: The series included 67 patients (27 men and 40 women) with no significant differences in distribution by sex or age group (19 to 59 years: 31.3%; 60 to 74 years: 37.4%; 75 years and older: 31.3%; p = 0.321). No significant differences were found in hematocrit values between the three time points (Friedman test, F = 0.363). All ICCs were greater than 0.8, indicating excellent agreement, with the highest agreement between measurements at 30 minutes and 6 hours (ICC = 0.897). Bland-Altman analysis showed a close mean difference between these two time points, with no systematic bias.
Conclusion: Hematocrit measurement at 30 minutes post-transfusion is adequate and reliable for representing the effect of the transfused unit; it shows excellent agreement with subsequent measurements.
Keywords: erythrocyte transfusion; hematocrit; patient care; reproducibility of results.
Recibido: 25/11/2025
Aprobado: 14/01/2026
INTRODUCCIÓN
La transfusión de concentrados de eritrocitos es una intervención terapéutica necesaria en la práctica médica hospitalaria, destinada a restaurar la capacidad de transporte de oxígeno en pacientes anémicos crónicos o con pérdida sanguínea aguda.(1) La evaluación de su eficacia se realiza de forma tradicional mediante la medición del hematocrito (Hto) o la determinación de la hemoglobina (Hb) después de la transfusión. La medición de estos parámetros entre 6 y 24 horas de finalizada la transfusión es una práctica clínica de amplia difusión, pero con un respaldo bibliográfico deficiente.(2,3)
Esta demora puede retrasar decisiones médicas críticas, como la necesidad de transfundir unidades adicionales o el alta hospitalaria, por lo que impacta en la eficiencia de los servicios de salud, sobre todo en contextos con recursos limitados.(3,4) En correspondencia con aspectos fisiopatológicos, los eritrocitos transfundidos permanecen en el espacio intravascular tras su infusión. Se espera que el equilibrio y la mezcla con el volumen sanguíneo del receptor ocurran en un período de tiempo corto.(1,5) Estudios recientes en diversas poblaciones, desde neonatos hasta adultos, han desafiado el paradigma de las 24 horas, al mostrar que los niveles de Hto y Hb se estabilizan a los 15 minutos, 1 hora o 4 horas postransfusión, sin diferencias significativas con respecto a la medición a las 24 horas.(5,6,7,8)
A pesar de que la evaluación del hematocrito postransfusional es una práctica clínica establecida desde hace décadas, la persistencia de protocolos basados en tradición más que en evidencia actualizada revela una paradoja significativa: si bien el tema no es novedoso, la literatura reciente es escasa y heterogénea. Esta escasez no obedece a que la cuestión haya perdido vigencia; por el contrario, la optimización del seguimiento transfusional sigue siendo crucial para la eficiencia clínica y la seguridad del paciente, especialmente en contextos de alta demanda y recursos limitados.(6,7,9)
La falta de estudios contemporáneos puede atribuirse a una presunción de resolución del problema, lo que ha generado un estancamiento en la generación de nuevas evidencias. Sin embargo, los avances en medicina transfusional y las crecientes presiones sobre los sistemas de salud exigen una reevaluación de prácticas rutinarias. Así, este estudio no solo busca llenar un vacío bibliográfico, sino también proporcionar datos robustos que permitan actualizar protocolos obsoletos, reducir demoras en la toma de decisiones y mejorar la calidad asistencial, al demostrar que la investigación en temas aparentemente consolidados sigue siendo esencial para la evolución de la medicina basada en evidencia.(2,8,9)
Por lo tanto, este estudio tuvo como objetivo determinar el momento óptimo (30 min, 6 h, 24 h) para medir el hematocrito en el seguimiento postransfusional.
MÉTODOS
Diseño y contexto
Se realizó un estudio observacional, longitudinal y prospectivo de evaluación tecnológica, en el Hospital Militar "Dr. Mario Muñoz Monroy" de Matanzas, Cuba, entre el 1ro de febrero y el 30 de abril de 2025.
Población y muestra
Análisis de poder muestral: previo al inicio del reclutamiento, se realizó un cálculo de tamaño muestral utilizando el software G*Power 3.1. Para detectar una diferencia clínicamente relevante de 3 puntos porcentuales en el hematocrito entre los tiempos de medición (se consideró una desviación estándar de 5 puntos, basada en datos piloto y literatura previa,(2,6) con un poder estadístico (1-β) del 80 % y un nivel de significación (α) de 0,05; se estimó un tamaño mínimo requerido de 54 pacientes. El reclutamiento de 67 pacientes superó este requerimiento, lo que asegura un poder adecuado para detectar diferencias del tamaño especificado (mayores a 3 %).
Se incluyeron de forma consecutiva todos los pacientes que recibieron transfusión de una unidad de concentrado de eritrocitos durante el periodo de estudio. Los criterios de exclusión fueron: 1) negativa a participar (ausencia de consentimiento informado por escrito); 2) no finalizar el protocolo de estudio (pérdida durante el seguimiento); 3) evidencia de sangrado activo o hemólisis durante el periodo de observación; 4) diagnóstico de insuficiencia cardíaca congestiva descompensada (clase NYHA III-IV) o síndrome nefrótico activo en el momento de la transfusión, debido a las alteraciones en la distribución de volumen asociadas.
Variables y procedimientos
A cada paciente se le realizaron tres mediciones de Hto después de finalizar la transfusión: a los 30 minutos, 6 horas y 24 horas. Las variables recogidas incluyeron: edad (años, estratificada en: 19 a 59 años, 60 a 74 años, 75 años y más), sexo, y los valores de Hto en los tres momentos definidos.
Procedimiento transfusional estandarizado: todas las unidades de concentrado de eritrocitos fueron administradas según el protocolo institucional. Se registraron y controlaron las siguientes variables: 1) volumen de la unidad transfundida (mL), obtenido del banco de sangre; 2) tipo y volumen de solución acompañante para la infusión (exclusivamente solución salina al 0,9 %); 3) velocidad de infusión, estandarizada a ≈ 2 mL/kg/hora para la mayoría de los pacientes, salvo indicación médica específica en cuyo caso se registró la velocidad real; y 4) tiempo total de transfusión (minutos).
Medición del hematocrito (estandarización analítica): para garantizar la consistencia y minimizar la variabilidad técnica, todas las determinaciones de hematocrito se realizaron mediante el mismo método y equipo. La medición se efectuó a partir de muestras de sangre venosa periférica recolectadas en tubos con EDTA-K2. El hematocrito fue determinado de forma manual, por micrométodo, con la centrifuga para microhematocrito KOKUSAN H1200F, en el laboratorio clínico central del hospital. El equipo estuvo sujeto a los controles de calidad rutinarios establecidos por el laboratorio.
Análisis estadístico
Los datos se procesaron con el software IBM-SPSS v.27. Las variables categóricas se describieron con frecuencias absolutas y relativas (n y %), y las proporciones se compararon con la prueba de ji cuadrado. Para comparar los valores medios de Hto en las tres mediciones (muestras relacionadas) se utilizó la prueba no paramétrica de Friedman para análisis de la varianza por rangos. La concordancia entre las mediciones se evaluó mediante el coeficiente de correlación intraclase (CCI) y se utilizó el gráfico de Bland-Altman para visualizar los sesgos y la dispersión entre los pares de mediciones. Se trabajó con un nivel de significación de p< 0,05 y un intervalo de confianza del 95 %.
Consideraciones éticas
La investigación fue aprobada por el Comité de Ética del Hospital Militar "Dr. Mario Muñoz Monroy". Todos los participantes firmaron un consentimiento informado por escrito.
RESULTADOS
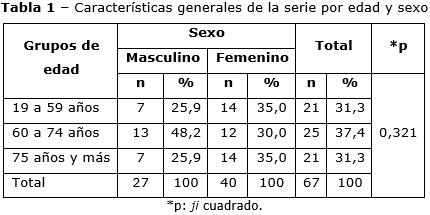
Participaron 67 pacientes con edad promedio de 68,2 ± 12,5 años; no hubo diferencias significativas en la distribución por sexo (40 mujeres, 27 hombres) ni por grupos etarios (hasta 59 años: 31,3 %; 60 a 74 años: 37,4 %; 75 años y más: 31,3 %; p= 0,321). La tabla 1 resume estas características generales.
La prueba de Friedman no reveló diferencias significativas entre las medianas de los valores de Hto a los 30 minutos, 6 horas y 24 horas postransfusión (F= 0,363; p≈ 0,84), lo que indica estabilidad en los valores de Hto durante el periodo estudiado (Fig. 1).
Los análisis de concordancia mostraron CCI superiores a 0,80 en todos los pares de comparaciones (tabla 2). El mayor coeficiente se observó entre las mediciones a los 30 min/6 h (CCI= 0,897; IC: 0,839-0,936), seguido de 6 h/24 h (CCI= 0,885; IC: 0,820-0,928) y 30 min/24 h (CCI= 0,845; IC: 0,759-0,902). Esto indica elevada similitud entre las muestras.
El gráfico de Bland-Altman para la comparación entre los valores de Hto a los 30 minutos y a las 6 horas mostró una diferencia media cercana a cero, lo que indica ausencia de un sesgo sistemático relevante entre ambas mediciones (Fig. 2). La gran mayoría de las diferencias individuales se situaron dentro de los límites de acuerdo (± 1,96 desviaciones estándar), esto refleja una buena concordancia y variabilidad mínima. No se observó una tendencia clara que indicara un aumento o disminución de las diferencias en función del nivel promedio de Hto.
DISCUSIÓN
El presente estudio demuestra que el hematocrito postransfusional se mantiene estable desde los 30 minutos hasta las 24 horas después de la transfusión, sin encontrar diferencias significativas entre estos momentos. Estos hallazgos se corresponden con investigaciones previas que cuestionan la necesidad de esperar 24 horas para evaluar el efecto de la transfusión.(8,10)
Karndumri K y otros,(2) en un estudio prospectivo con 60 pacientes, no encontraron diferencias significativas en el Hto a las 1, 4 y 24 horas postransfusión, por lo que concluyeron que el objetivo de la transfusión puede determinarse desde la primera hora. Estos resultados respaldan el hallazgo de alta concordancia entre 30 min y 6 h (CCI= 0,897) en el trabajo que se presenta, reforzada por el análisis de Bland-Altman sin sesgo importante. Al contrario, Audu LI y otros(8) reportaron en neonatos que la estabilización real ocurre cerca de las 12 horas, lo que resalta la posible variabilidad según la edad y el contexto.
La alta concordancia, en particular entre los 30 minutos y las 6 horas es el hallazgo más robusto de la actual investigación, lo cual coincide con estudios anteriores.(2,5) Esto sugiere que la medición a los 30 minutos es tan confiable como la realizada a las 6 horas para representar el efecto agudo de la transfusión. La implementación de esta práctica permitiría una toma de decisiones más ágil, por ejemplo, indicar transfusiones adicionales o autorizar el alta. De este modo se optimizaría el uso de camas hospitalarias y recursos diagnósticos, sobre todo en instituciones con alta demanda de servicios.(6)
Este estudio tiene como limitación que la serie, aunque suficiente para el análisis estadístico, fue obtenida en un solo centro hospitalario, lo cual puede restringir la generalización de los resultados. Sería necesario validar estos hallazgos en muestras multicéntricas y estratificadas: para evaluar la homogeneidad de la muestra y la posible influencia del contexto clínico según el escenario principal que motivó la transfusión; por ejemplo, pacientes con inestabilidad hemodinámica o comorbilidades específicas.
En conclusión, los resultados de este estudio demuestran que la medición del hematocrito a los 30 minutos postransfusión es adecuada y confiable para representar el efecto de la unidad transfundida, con una excelente concordancia respecto a mediciones después de las 6 y 24 horas. Se recomienda revisar los protocolos de práctica clínica para incorporar la medición temprana a los 30 minutos del Hto, lo que contribuiría a una asistencia más eficiente y centrada en el paciente.
Se recomienda incluir mediciones de Hto previas, 30 minutos después de la transfusión, para determinar si la estabilización ocurre incluso antes del periodo estudiado.
Agradecimientos
El equipo de trabajo agradece la colaboración del personal del laboratorio clínico y del banco de sangre del Hospital Militar "Dr. Mario Muñoz Monroy" por su invaluable apoyo en la recolección de las muestras. A Aida M. Jiménez Bosco y Juan R. Peña Santana por la revisión del artículo.
REFERENCIAS BIBLIOGRÁFICAS
1. Carson JL, Guyatt G, Heddle NM, Grossman BJ, Cohn CS, Fung MK, et al. Clinical Practice Guidelines From the AABB: Red Blood Cell Transfusion Thresholds and Storage [Internet]. JAMA. 2016;316(19):2025-35. DOI: 10.1001/jama.2016.9185
2. Karndumri K, Tantiworawit A, Hantrakool S, Fanhchaksaic K, Rattarittamrong E, Limsukond A, et al. Comparison of hemoglobin and hematocrit levels at 1, 4 and 24 h after red blood cell transfusion. [Internet]. Transfus Apher Sci. 2020;59:102586. DOI: 10.1016/j.transci.2019.06.021
3. Wiesen AR, Hospenthal DR, Byrd JC, Glass KL, Howard RS, Diehl LF. Equilibration of hemoglobin concentration after transfusion in medical inpatients not actively bleeding [Internet]. Ann Intern Med. 1994;121(4):278-80. DOI: 10.7326/0003-4819-121-4-199408150-00009
4. Elizalde JI, Clemente J, Marín JL, Panés J, Aragón B, Mas A, et al. Early changes in hemoglobin and hematocrit levels after packed red cell transfusion in patients with acute anemia [Internet]. Transfusion. 1997;37(6):573-6. DOI: 10.1046/j.1537-2995.1997.37697335151.x
5. Lichtman MA, Kaushansky K, Prchal JT, Levi MM, Burns LJ, Armitage JO. Williams Hematology, 10th edition. New York: McGraw-Hill Education; 2021 [acceso: 30/07/2025]. Disponible en: https://accessmedicine.mhmedical.com/book.aspx?bookid=2962
6. Adeleye QA, Oniyangi O, Audu LI. The earliest time for haematocrit check after packed red blood cell transfusion among children with anaemia [Internet]. South Afr J Child Health. 2021;15(3):137-41. DOI: 10.7196/SAJCH.2021.v15.i3.1772
7. Enya VE, Orji MLC, Brown BJ. Equilibration time of haemoglobin concentration after packed red blood cell transfusion in children seen in the emergency unit of a tertiary hospital in Southeast, Nigeria [Internet]. Transfus Apher Sci. 2023;62(4):103709. DOI: 10.1016/j.transci.2023.103709
8. Audu LI, Otuneye AT, Mairami AB, Mshelia LJ, Nwatah VE. Posttransfusion haematocrit equilibration: timing posttransfusion haematocrit check in neonates at the national hospital, Abuja, Nigeria [Internet]. Int J Pediatr. 2015;2015:175867. DOI: 10.1155/2015/175867
9. Sekhsaria S, Fomufod A. Readjustment of hematocrit values after packed red cell transfusion in the neonate. J Perinatol. 1991 [acceso: 31/07/2025];11(2):161-3. Disponible en: https://pubmed.ncbi.nlm.nih.gov/1890477/
10. Glatstein M, Oron T, Barak M, Mimouni FB, Dollberg S. Posttransfusion equilibration of hematocrit in hemodynamically stable neonates [Internet]. Pediatr Crit Care Med. 2005;6(6):707-8. DOI:10.1097/01.PCC.0000185490.19677.B4
Conflictos de interés
Los autores declaran que no existen conflictos de interés relacionados con este estudio.
Información financiera
No se recibió financiamiento específico para la realización de este trabajo.
Contribuciones de los autores
Conceptualización: Leydiana Trimiño Galindo, Junior Vega Jiménez, Rubén González Tabares.
Curación de datos: Leydiana Trimiño Galindo, Junior Vega Jiménez, Rubén González Tabares.
Análisis formal: Leydiana Trimiño Galindo, Junior Vega Jiménez, Rubén González Tabares.
Investigación: Leydiana Trimiño Galindo, Junior Vega Jiménez, Rubén González Tabares, Layanis Guardarrama Linares, Lisneybi González González.
Metodología: Leydiana Trimiño Galindo, Junior Vega Jiménez, Rubén González Tabares, Layanis Guardarrama Linares, Lisneybi González González.
Redacción - borrador original: Leydiana Trimiño Galindo, Junior Vega Jiménez, Rubén González Tabares, Layanis Guardarrama Linares, Lisneybi Gonzalez Gonzalez.
Redacción - revisión y edición: Leydiana Trimiño Galindo, Junior Vega Jiménez, Rubén González Tabares, Layanis Guardarrama Linares, Lisneybi Gonzalez Gonzalez.
Disponibilidad de datos
Los datos que respaldan los hallazgos de este estudio están disponibles en el Hospital Militar "Dr. Mario Muñoz Monroy", pero tienen restricciones de confidencialidad según las políticas institucionales, por lo que no son de acceso público. Sin embargo, los datos están disponibles para los revisores previa solicitud razonable y con la autorización de la institución.