Artículo de Revisión
El pez cebra como biomodelo en oncología, aplicaciones en la evaluación de terapias y vectores génicos
Zebrafish as a biomodel in oncology, applications in the evaluation of therapies and gene vectors
Thalía Sánchez Miralles1 https://orcid.org/0009-0008-5844-7418
Sheyla Fernández Puentes1 https://orcid.org/0000-0001-5202-5291
Kamila Morín Fanego1 https://orcid.org/0000-0002-0042-3834
Yenia Aldana Mulet1 https://orcid.org/0009-0007-0870-5725
Dianelys Cabrera Márquez1 https://orcid.org/0009-0008-9684-5230
Anabel Cisneros Campo1 https://orcid.org/0009-0006-6964-1836
Sonia García Lago1 https://orcid.org/0009-0001-3012-5176
Silvia García Viamonte1 https://orcid.org/0009-0001-8919-4096
Luis Arturo Fonseca-Fonseca¹ https://orcid.org/0000-0001-6904-5854
Jorge Berlanga Acosta2 https://orcid.org/0000-0001-9797-1986
Ché Serguera3 https://orcid.org/0000-0002-9210-0636
Yanier Nunez-Figueredo1* https://orcid.org/0000-0001-5633-4518
1Centro de Investigación y Desarrollo de Medicamentos. Laboratorio de Neurofarmacología Experimental. La Habana, Cuba.
2Centro de Ingeniería Genética y Biotecnología (CIGB). La Habana, Cuba.
3Sorbonne Université. Institut du Cerveau. Asfalia Biologics. Paris, France.
*Autor para la correspondencia. Correo electrónico: yanier.nunez@cidem.cu
RESUMEN
Introducción: El pez cebra (Danio rerio) se ha consolidado como un modelo biológico fundamental en medicina experimental y oncología, gracias a su elevada homología genética con humanos (82 % en genes asociados a enfermedades), transparencia embrionaria y facilidad de manipulación genética.
Objetivo: Revisar el papel del pez cebra en la investigación oncológica, su aplicación para el estudio de la progresión tumoral y relevancia en áreas innovadoras, como las terapias genéticas.
Métodos: Se realizó una revisión de la literatura científica actual, analizando estudios que emplean al pez cebra como modelo en oncología. Se descartaron estudios sin validación experimental relevante, artículos de opinión sin base empírica, o investigaciones que no establecían correlación con modelos de cáncer humano.
Desarrollo: La transparencia del modelo y el desarrollo de líneas transgénicas facilitan la observación directa y el seguimiento de células tumorales. En terapia génica, el pez cebra ha sido instrumental para probar y optimizar sistemas de transferencia de genes terapéuticos, tanto virales como no virales. Además, su uso en estudios preclínicos ha permitido validar terapias innovadoras, como células CAR-T y estrategias de edición genómica con CRISPR/Cas9, aceleran el desarrollo de tratamientos dirigidos.
Conclusiones: El pez cebra constituye un modelo vertebrado clave para la oncología, permite visualizar en tiempo real la progresión tumoral y la interacción con el microambiente, a la vez que su alta factibilidad para la edición génica lo posiciona como una plataforma central en el desarrollo de terapias génicas innovadoras.
Palabras clave: modelo biológico; pez cebra; oncología; terapias genéticas.
ABSTRACT
Introduction: Zebrafish (Danio rerio) has become a fundamental biological model in experimental medicine and oncology due to its high genetic homology with humans (82% in disease-associated genes), embryonic transparency, and ease of genetic manipulation.
Objective: To review the role of zebrafish in cancer research, focusing on its application for studying tumor progression and its relevance in innovative areas such as gene therapies.
Methods: A review of current scientific literature was conducted, analyzing studies that use zebrafish as a model in oncology. Studies without relevant experimental validation, opinion articles without empirical basis, or research that did not establish correlation with human cancer models were excluded.
Development: The transparency of the model and the development of transgenic lines facilitate direct observation and tracking of tumor cells. In gene therapy, zebrafish has been instrumental in testing and optimizing therapeutic gene delivery systems, both viral and non-viral. Furthermore, its use in preclinical studies has enabled the validation of innovative therapies, such as CAR-T cells, and genome editing strategies with CRISPR/Cas9, accelerating the development of targeted treatments.
Conclusions: Zebrafish constitutes a key vertebrate model for oncology, allowing real-time visualization of tumor progression and interaction with the microenvironment, while its high feasibility for gene editing positions it as a central platform in the development of innovative gene therapies.
Keywords: biological model; gene therapies; oncology; zebrafish.
Recibido: 21/01/2026
Aprobado: 10/04/2026
INTRODUCCIÓN
El sistema inmunológico constituye la principal defensa del organismo contra agentes nocivos, aunque en enfermedades como el cáncer su función se compromete por alteraciones celulares complejas, que incluyen mutaciones genéticas, reordenamientos cromosómicos y cambios epigenéticos.(1,2) La incidencia del cáncer ha aumentado rápidamente en las últimas décadas; se proyecta un incremento del 60 % para 2045 en la región de las Américas según la Organización Mundial de la Salud (OMS - https://www.paho.org/es/temas/cancer).
La conexión entre cáncer e inmunología, establecida desde Virchow,(3) se fundamenta en el ciclo de inmunidad antitumoral, en el cual células presentadoras de antígenos activan linfocitos T citotóxicos, que eliminan células tumorales mediante perforina y granzima.(4) Aunque el ciclo de inmunidad contra el cáncer es un mecanismo eficaz, las células tumorales pueden evolucionar de manera progresiva, lo que evidencia su habilidad para evadir la vigilancia inmunológica.(4) Este fenómeno indica que los tumores malignos desarrollan estrategias para evadir el rechazo inmunitario. Mientras que en el pasado el arsenal terapéutico se limitaba principalmente a la cirugía, la radioterapia y la quimioterapia convencional; el panorama actual incluye diversas modalidades de tratamiento más específicas, como las terapias dirigidas y, más recientemente, los enfoques de inmunoterapia que están revolucionando el manejo de estas enfermedades.(5) Por otra parte, la terapia génica ha emergido como alternativa eficaz para cánceres hematológicos, mediante la introducción controlada de material genético que corrige defectos moleculares.(6) Su eficacia se potencia al combinarse con tratamientos convencionales y muestra resultados prometedores en cáncer de mama, pulmón y cuello uterino.(7,8,9) El principal desafío radica en la entrega eficiente del gen terapéutico, superado mediante vectores, que protegen el material genético y facilitan su internalización.(10,6) Hoy día, el campo de la medicina que más emplea la terapia génica es la oncología, con la fabricación ex vivo de linfocitos T genéticamente modificados, para expresar un receptor del antígeno quimérico (CAR en inglés); estos han demostrado eficacia notable en linfomas y leucemias refractarias,(11) que favorece el desarrollo de CAR contra nuevos antígenos tumorales.(12)
Los modelos animales desempeñan un papel fundamental en la investigación biomédica preclínica; permiten el estudio de los procesos patológicos asociados a diversas enfermedades y evaluar nuevas estrategias terapéuticas. Entre estos modelos, el pez cebra (Danio rerio) ha surgido como un organismo particularmente valioso para investigar enfermedades humanas, como cáncer, trastornos cardiovasculares, enfermedades neurodegenerativas y procesos de angiogénesis. La relevancia se debe, en parte, a la alta homología genética (76-82 %) entre el pez cebra y los humanos, especialmente en genes relacionados con enfermedades. Además, la disponibilidad de múltiples líneas transgénicas simplifica su uso en ensayos experimentales, lo que permite optimizar su aplicabilidad en estudios biomédicos.(13)
El presente artículo tiene como objetivo revisar el papel del pez cebra en la investigación oncológica, centrando en su aplicación para el estudio de la progresión tumoral y relevancia en áreas innovadoras, como las terapias genéticas.
MÉTODOS
Se realizó una búsqueda integradora de literatura científica en las bases de datos PubMed, Scopus y a través de Google académico; se utilizaron los términos clave: "Zebrafish cancer model", "Danio rerio gene therapy", "zebrafish xenograft", "anticancer drug screening in zebrafish" y sus equivalentes en español.
La búsqueda abarcó artículos publicados entre 2000 y 2025. Arrojó inicialmente 150 artículos, los cuales se filtraron con prioridad a estudios originales, revisiones sistemáticas y metaanálisis que abordaran el uso del pez cebra en la investigación oncológica y desarrollo de terapias génicas. Los criterios de inclusión fueron:
Aplicabilidad traslacional clara (estudios que vincularan hallazgos en pez cebra con mecanismos o resultados en modelos humanos o líneas celulares humanas).
Diseño experimental robusto y descrito.
Validación de los hallazgos mediante métodos complementarios.
Publicación en revistas de alto impacto.
Se descartaron estudios sin validación experimental relevante; artículos de opinión sin base empírica, o investigaciones que no establecían correlación con modelos de cáncer humano. Tras este proceso, se incluyeron 93 referencias como base principal para el análisis y la discusión presentada en esta revisión.
DESARROLLO
El pez cebra como biomodelo experimental
El pez cebra (Danio rerio) se estableció como organismo modelo, gracias a los trabajos del genetista George Streisinger durante la década de los ochenta del siglo XX, cuyos estudios demostraron por primera vez su potencial para procesos biológicos humanos. Después, en 1996, equipos científicos de EE. UU. y Alemania identificaron mutaciones génicas clave en esta especie; para el año 2000 se logró la secuenciación completa de su genoma y consolidar su relevancia en la investigación biomédica.(14) El conocimiento detallado del genoma de este organismo impulsó la generación de modelos biológicos capaces de simular diversas afecciones humanas.
El desarrollo embrionario del pez cebra presenta notables similitudes con el de los vertebrados superiores, incluyendo la especie humana. Este organismo ofrece ventajas significativas frente a otros modelos animales, como los ratones: Reducido tamaño, facilidad para modificaciones genéticas y rápida reproducción; que permiten mantener colonias numerosas, con requerimientos económicos mínimos.(15) El ciclo ontogénico presenta notable rapidez, durante el cual un cigoto unicelular evoluciona a un embrión móvil y ópticamente transparente en apenas 24 horas. La organogénesis principal culmina aproximadamente a los tres días postfecundación (dpf), mientras que la funcionalidad del tracto digestivo y estructuras bucales se establece entre los días 5-6 dpf.(16)
Durante la fase embrionaria y larval inicial, los recursos nutricionales del saco vitelino se movilizan de forma eficiente, para su reabsorción hacia el séptimo día de desarrollo. La transición a estadio juvenil ocurre al adquirir la morfología definitiva, por lo que alcanzan la madurez sexual cuando desarrollan capacidad reproductiva activa.(16) Bajo condiciones controladas de laboratorio, el pez cebra alcanza su madurez reproductiva a los tres meses de vida. Este organismo presenta una homología genética de ~70 % con el genoma humano, que asciende al 82 % en genes asociados a enfermedades, lo que valida su utilidad como sistema modelo para investigación traslacional en biomedicina.(14)
Estas ventajas posicionan al pez cebra como un modelo experimental valioso en la investigación biomédica, lo que facilita estudios de desarrollo, enfermedades y terapias de manera eficiente y rentable.
El pez cebra como herramienta en el campo oncológico
Ventajas para estudios carcinogénicos
Para que un organismo sea considerado como modelo de estudio es fundamental que presente un alto grado de conservación genética, en los genes de interés, en comparación con la especie bajo investigación. En el caso del pez cebra, numerosos mecanismos asociados al desarrollo del cáncer muestran una notable similitud con los humanos. Varias marcas epigenéticas, encargadas de regular la expresión de los genes, se mantienen conservadas en especies vertebradas como el pez cebra y los seres humanos.(5) El pez cebra comparte genes relacionados con el ciclo celular; también mantiene conservados oncogenes y genes supresores de tumores, que lo convierten en un modelo ideal para investigar rutas oncogénicas y realizar seguimientos específicos en estudios de cáncer.(17)
Otra ventaja clave es su manipulación genética sencilla. Gracias a la transparencia de sus embriones, es posible la observación directa de la expresión y localización de genes introducidos experimentalmente. Además, la microinyección de material genético en etapas tempranas (como la fase unicelular) facilita técnicas como knockout génico, sobreexpresión y transgénesis. Estas herramientas permiten desarrollar y analizar con precisión modelos de cáncer basados en alteraciones genéticas.(13)
Entre los modelos transgénicos de pez cebra existentes, se destacan líneas con marcadores específicos en ciertos tejidos (como macrófagos(18) neutrófilos(19) o vasos sanguíneos(20)), así como variedades con inmunodeficiencia o falta de pigmentación.(21) Un caso particularmente relevante es la línea Casper, conocida por su transparencia. Esta característica, sumada a la posibilidad de introducir células tumorales o proteínas fluorescentes, la convierte en un sistema excepcional para estudiar procesos oncológicos. Con este modelo, los investigadores pueden monitorear en tiempo real la progresión de tumores, los mecanismos de invasión metastásica, e incluso evaluar la eficacia de terapias antitumorales.(22) Facchinello N y otros(23) reportaron que los tumores humanos trasplantados en el pez cebra reproducen fielmente las características histopatológicas de los tumores primarios en pacientes.
Sistema inmunológico
Al igual que ocurre en las personas, el pez cebra cuenta con un sistema inmunitario complejo, que incluye dos ramas principales, ambas con elementos innatos y adaptativos perfectamente desarrollados. De hecho, estos peces tienen dos órganos linfoides primarios clave. Por un lado, está la médula renal, que sería el equivalente a la médula ósea humana. Por otro, el timo, que con la edad se reduce, tanto en estos peces como en los seres humanos. Además, poseen un órgano linfoide secundario periférico: El bazo.(24) Sin embargo, hay una distinción clave en los órganos inmunitarios secundarios: A diferencia de los humanos, el pez cebra no tiene ganglios linfáticos. Entonces, las interacciones inmunes más importantes ocurren principalmente en el bazo, que actúa como el escenario central en el cual las células presentadoras de antígenos y los linfocitos se comunican y coordinan la respuesta defensiva.(25)
Al igual que en los mamíferos, el pez cebra expresa moléculas del complejo mayor de histocompatibilidad (clase I y II), lo que demuestra que su sistema inmunitario conserva mecanismos similares para coordinar las defensas innatas y adaptativas. En el caso del pez cebra, su inmunidad adaptativa se activa de forma progresiva: Entre la tercera y sexta semana de desarrollo ya cuentan con células T y B completamente funcionales.(26) Las células T se desarrollan en el timo, tanto en las larvas como en los adultos, aunque en los peces maduros estas migran y se alojan en la médula renal. Por otro lado, los linfocitos B tienen un origen distinto: En las larvas se forman en el pronefros, mientras que en los adultos dependen de la médula renal. Es curioso que aunque los linfocitos B aparecen desde la tercera semana de desarrollo, solo alcanzan su plena madurez y capacidad funcional en la sexta semana.(25) La breve ventana de incompetencia inmunológica permite desarrollar técnicas relacionadas con estudios de cáncer, como los carcinogénicos y el xenotrasplante.
Xenotrasplantes en pez cebra
Xenoinjerto en embriones y larvas
La investigación oncológica enfrenta limitaciones éticas y técnicas que justifican el uso de organismos modelo. Los xenotrasplantes, que consisten en trasplantar material biológico entre especies diferentes, permiten estudiar enfermedades humanas en animales, sin poner en riesgo a pacientes.(27) En este contexto, se implantan células cancerosas humanas en organismos de menor tamaño, se recrean aspectos de la enfermedad, aunque sin constituir un modelo animal de esta.(28)
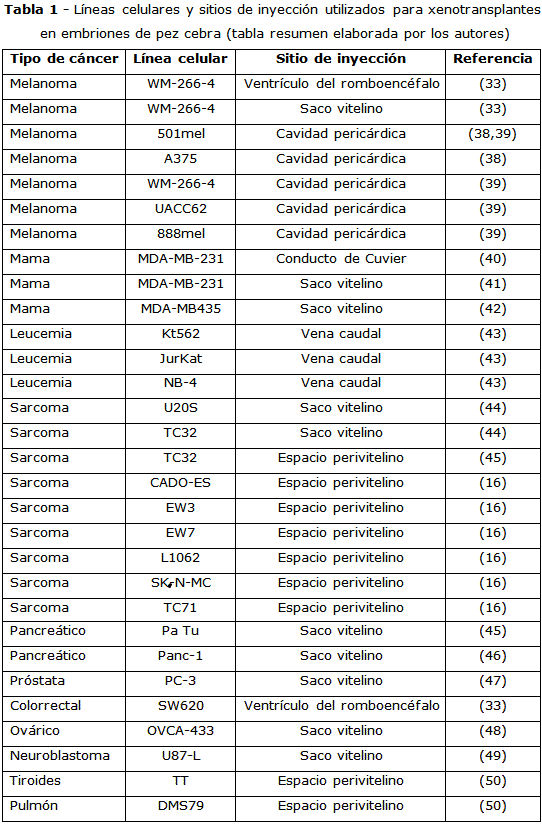
El pez cebra presenta características únicas para estudios de trasplante: Embriones de desarrollo rápido y transparente, que facilitan la observación directa de procesos celulares, posibilidad de rastreo con fluorescencia, y maduración tardía de su sistema inmunitario adaptativo, lo que evita el rechazo de tejidos durante las primeras seis semanas de vida.(29) Además, el establecimiento de xenotrasplantes en pez cebra requiere solo días o semanas, a diferencia de los modelos murinos, que tardan semanas o meses.(30) La tabla 1 resume algunas de las líneas celulares trasplantadas y los sitios de inyección empleados.
En 2005 se logró el primer xenotrasplante de melanoma humano en pez cebra.(31) Dos años después se adaptó el modelo en larvas de 1 dpf para estudiar tumorigénesis, metástasis y angiogénesis.(32) Haldi M y otros(33) establecieron en 2006 los parámetros clave para estos procedimientos; identificaron el saco vitelino de embriones de 2 dpf, como sitio óptimo de inyección por su ambiente acelular, que favorece la nutrición celular, desarrollo tumoral y migración. Esta localización continúa siendo la principal elección para xenotrasplantes embrionarios.(34)
Algunos estudios respaldan el valor del pez cebra como modelo preclínico en oncología.(35,36) Los xenotrasplantes en embriones permiten evaluar in vivo la eficacia de terapias como células CAR-T contra neoplasias humanas, con ventajas de rapidez, bajo costo y seguimiento por imagenología en tiempo real.(35) Aunque la temperatura óptima para el pez cebra es 26-28 °C, los embriones con xenotrasplantes pueden mantenerse hasta 34 °C para emular condiciones fisiológicas humanas.(21,37) Sin embargo, el modelo presenta limitaciones: Ventana experimental de ~7 días, capacidad restringida a 100-200 células por individuo, dificultad para incluir poblaciones como células madre tumorales, limitada representación de la heterogeneidad genética y respuestas farmacológicas de subclones minoritarios característicos de tumores humanos.(36)
Xenoinjertos en peces cebra adultos
En el pez cebra adulto, para implantar células tumorales humanas, se realiza sobre todo, mediante inyección intraperitoneal. No obstante, este procedimiento solo es viable en organismos inmunodeprimidos, ya que el sistema inmunitario del pez adulto, compuesto por linfocitos y células presentadoras de antígenos, reconoce y elimina eficientemente las células tumorales xenógenas, de forma similar a lo observado en modelos mamíferos.(51,52) Por ende, para garantizar el éxito del trasplante en el pez cebra adulto, es necesario suprimir la respuesta inmunitaria del huésped, mediante técnicas como irradiación, tratamiento con agentes inmunosupresores o inducción de mutaciones genéticas que afecten a la función de las células T.(25)
Los avances recientes en modelos animales han permitido el desarrollo de cepas inmunodeficientes de pez cebra, capaces de recibir trasplantes de células tumorales humanas procedentes directamente de pacientes. Aunque estos sistemas, al inicio demostraron capacidad para mantener injertos tumorales funcionales, durante aproximadamente un mes postrasplante, su eficacia se ve comprometida por los efectos colaterales asociados a los métodos de inmunosupresión empleados. Frente a estos desafíos, el laboratorio de David M. Langenau, en Harvard, creó un innovador sistema, con el uso de la variedad Casper de pez cebra, en el cual, mediante la generación de mutaciones homocigóticas knockout se consiguió un modelo optimizado, para el mantenimiento prolongado de xenoinjertos, tanto humanos como murinos.(21) Recientemente desarrollados, estos peces mutantes presentan una combinación única de características: Transparencia óptica, ausencia completa de linfocitos T, B y células NK (Natural Killer), junto con notable tolerancia a la temperatura humana (37 °C). Estudios de viabilidad confirmaron que, mediante protocolos de aclimatación gradual y manejo especializado, los especímenes mutantes mantienen altas tasas de supervivencia en condiciones fisiológicas humanas. Esta plataforma innovadora ha demostrado ser particularmente eficaz para el mantenimiento prolongado (más de 4 semanas), de diversos tipos de neoplasias humanas, lo que permite el estudio continuo de su progresión y comportamiento in vivo.(21)
El empleo de peces cebra adultos en xenotrasplantes ofrece ventajas notables; se destaca la capacidad de injertar un volumen celular mucho mayor (hasta dos millones de células) en comparación con otros modelos. Este modelo experimental no solo permite prolongar el período de observación, sino que facilita el mantenimiento de condiciones térmicas equivalentes a las humanas.(5)
Fármacos e inmunoterapia en pez cebra
El desarrollo de nuevos fármacos antitumorales implica procesos extensos y costosos, que inician con evaluaciones in vitro de parámetros como inhibición proliferativa, toxicidad selectiva y modulación de biomarcadores, para luego avanzar a estudios farmacocinéticos in vivo, que permiten la selección definitiva de candidatos terapéuticos.(53) El pez cebra posee una capacidad única para internalizar compuestos directamente del medio acuático, por lo que se considera un sistema superior a los roedores para estudios de farmacología y biodisponibilidad.(29) Su versatilidad lo posiciona como un puente experimental ideal entre cultivos celulares y modelos mamíferos, de esta manera acelera la identificación de agentes prometedores y confirma la eficacia de tratamientos antitumorales a lo largo de todo el espectro del desarrollo farmacéutico.(54) Este modelo ha demostrado efectividad en la evaluación de quimioterapéuticos convencionales, fármacos dirigidos como dasatinib y terapias biológicas con anticuerpos monoclonales como bevacizumab;(55) además de constituir una herramienta valiosa para probar compuestos contra el cáncer colorrectal, como cetuximab y regorafenib.(36) Esto aumenta las probabilidades de éxito en fases clínicas, mientras reduce costos y tiempo.(56)
El estudio del sistema linfático vascular, en el microambiente tumoral, mediante xenoinjertos en pez cebra, proporciona hallazgos valiosos para desarrollar nuevas estrategias de inmunoterapia, que incluyen inhibidores de puntos de control inmunológico.(2) La terapia CAR-T, que implica la modificación genética de linfocitos T para expresar receptores quiméricos que identifican antígenos tumorales específicos,(57) encuentra en el pez cebra un modelo particularmente adecuado para su evaluación preclínica. Durante su desarrollo larvario, este organismo genera de forma gradual, componentes clave del sistema inmunitario, como células T, B y NK, y adquiere así, tanto inmunidad innata como adaptativa, lo que permite utilizar modelos de xenoinjerto para evaluar la eficacia de terapias CAR-T in vivo.(4) La validación experimental del modelo se ha demostrado en estudios en los cuales células CAR-T anti-CD19 erradicaron eficientemente líneas de leucemia pre-B (Nalm-6) en embriones de pez cebra.(35) Implementar metodologías innovadoras para cuantificar dinámicamente la interacción entre células tumorales y células CAR-T, ha posicionado este sistema como una herramienta prometedora para la evaluación preclínica, gracias a su rapidez, bajo costo y alto potencial traslacional.(35)
Terapia génica
Aspectos generales
La terapia génica introduce ácidos nucleicos en células diana, para corregir alteraciones genéticas, modular la expresión génica o sustituir genes defectuosos.(58) Su aplicación ha evolucionado desde enfermedades monogénicas, hasta estrategias oncológicas, como inducción de apoptosis selectiva y síntesis de proteínas terapéuticas.(59,60) El principal desafío es la entrega eficiente del gen terapéutico, pues el ADN libre se degrada rápidamente y las células no lo internalizan con facilidad; requiere sistemas de transporte especializados.(10,61) Los vectores, clasificados en virales y no virales, facilitan este proceso.(61) Los virales transducen células en división y quiescentes, pero generan respuestas inmunogénicas; los no virales (nanopartículas y métodos físicos) presentan menor inmunogenicidad, aunque eficacia reducida.(62)
Estas plataformas se emplean en inmunoterapia, terapia génica suicida, regulación de miARN, CAR-T, inhibición de oncogenes y edición con CRISPR/Cas9.(63,64) Métodos físicos como electroporación y microinyección generan poros transitorios en membranas, para facilitar el paso de material genético;(10) aunque su eficacia de transfección es inferior a la viral.(65) La nanotecnología ha revolucionado la oncología mediante nanopartículas como vehículos inteligentes con direccionamiento activo o pasivo, que incrementan la concentración en células tumorales y reducen daño a tejidos sanos. Su versatilidad permite liberar la carga terapéutica al detectar condiciones específicas del microambiente tumoral (pH bajo o temperatura elevada),(66) mejorando la farmacocinética, precisión administración, reduciendo efectos adversos y disminuyendo resistencias a tratamientos.(67)
Vectores virales
Los vectores virales modificados genéticamente, para reemplazar genes patogénicos por transgenes,(6) ofrecen alta eficiencia en terapia génica. Se clasifican en integrativos (retrovirus y lentivirus) y episomales (adenovirus y virus adenoasociados). Los retrovirus (ej. MMLV) integran su material en el cromosoma huésped, pero presentan riesgo de mutagénesis insercional,(68) especialmente por su potencial oncogénico(69) y solo transducen células en división. Los lentivirus (derivados del VIH) superan esta limitación e infectan también células en reposo.(10) Han demostrado eficacia oncológica en carcinoma mamario(70) y neoplasias uroteliales,(71) siendo su principal uso clínico la modificación de linfocitos para terapia CAR-T en neoplasias hematológicas y enfermedades autoinmunes.(72)
Los adenovirus transducen eficientemente diversos tipos celulares(73) y activan la respuesta inmune en tumores sólidos,(74) aunque su inmunogenicidad limita otras aplicaciones.(6) Los virus adenoasociados (AAV) destacan por su seguridad, mínima reactogenicidad y genoma compacto,(75) con innovaciones en bioingeniería de cápsides, que amplía su precisión terapéutica(76) para enfermedades monogénicas, metabólicas y neurodegenerativas.(77)
Vectores no virales
Como alternativa más segura a los vectores virales, por su menor mutagenicidad e inmunogenicidad,(78,79) los sistemas no virales representan actualmente uno de cada seis ensayos clínicos en terapia génica. Los polímeros catiónicos como poli-L-lisina (PLL) y polietilenimina (PEI) muestran eficacia en transferencia génica in vitro;(80) destacan las formulaciones de PEI por su baja inmunogenicidad, versatilidad estructural y compatibilidad con múltiples tipos celulares para administrar ARN interferente (siRNA).(81) Las nanopartículas ofrecen perfil farmacológico mejorado y propiedades fisicoquímicas superiores. La formulación LCPP con TRAIL y sorafenib demostró eficacia en carcinoma hepatocelular y fibrosis asociada,(82) mientras que sistemas nanovehiculados para microARN terapéuticos han mostrado seguridad y eficacia contra CHC,(83) lo cual las posiciona como plataformas ideales para administración selectiva en oncología.(84) Adicionalmente, las nanopartículas modulan la respuesta inmunitaria antitumoral mediante inducción de muerte celular inmunogénica, remodelación del microambiente tumoral, eliminación de células inmunosupresoras, mejora en presentación antigénica y estimulación de la infiltración de linfocitos citotóxicos.(85)
Organismos modelo en terapia génica
Aunque los enfoques computacionales (in silico) y los cultivos celulares (in vitro) son herramientas valiosas para el estudio del cáncer, presentan limitaciones importantes al no poder replicar completamente la complejidad de un organismo vivo, especialmente en lo que respecta a los procesos metabólicos y los patrones de distribución de tumores invasivos.(86) Esta limitación subraya la importancia crítica de los modelos animales en la investigación preclínica; permiten evaluar con mayor precisión, tanto la seguridad como la eficacia de nuevas terapias. Organismos modelo como el nematodo C. elegans,(87) el pez cebra D. rerio,(88) la mosca de la fruta D. melanogaster(89) y el ratón M. musculus(90) han contribuido significativamente a desentrañar los mecanismos moleculares del cáncer y a optimizar los protocolos terapéuticos.
Entre estos modelos, el pez cebra destaca por características únicas, que lo hacen particularmente útil en oncología: Su rápido ciclo reproductivo, la transparencia corporal durante etapas tempranas de desarrollo y un genoma completamente secuenciado. Estas ventajas, sumadas a la conservación evolutiva de órganos y rutas metabólicas similares a las humanas, permiten realizar evaluaciones toxicológicas detalladas y estudios de biocompatibilidad.(91) La transparencia embrionaria facilita además el monitoreo no invasivo de nanopartículas, permiten caracterizar su distribución anatómica e interacciones con células tumorales, sin procedimientos invasivos.(92) Los modelos transgénicos de pez cebra representan un avance adicional, ya que permiten el seguimiento en tiempo real de células cancerosas, sin requerir técnicas de marcaje convencionales y evitan artefactos experimentales. La versatilidad de este modelo queda demostrada por su aplicación en el estudio de diversos tipos tumorales, incluyendo cánceres de pulmón, estómago, colon, ovario, cerebro, sangre, páncreas, próstata y piel.(6) Esta amplia aplicabilidad, combinada con sus ventajas técnicas, ha posicionado al pez cebra como un sistema biológico excepcional para desarrollar y validar terapias génicas innovadoras.(93)
El pez cebra (Danio rerio) emerge como un modelo revolucionario en investigación oncológica; destaca por su alto grado de conservación genética con humanos, versatilidad experimental y bajo costo. Se demuestra su triple utilidad: (1) Como plataforma ideal para xenotrasplantes, que permite estudiar metástasis y respuesta a terapias en tiempo real; (2) como sistema eficiente para validar algunas terapias génicas y (3) como herramienta útil para el cribado rápido de fármacos antitumorales.
Aunque presenta limitaciones en la reproducción de ciertos aspectos de la fisiología humana, su capacidad para reducir tiempos y costos en la investigación preclínica lo convierten en un eslabón de gran interés entre los estudios in vitro y los ensayos en mamíferos. El futuro de la oncología traslacional deberá integrar estratégicamente este modelo para acelerar el desarrollo de terapias personalizadas contra el cáncer, lo que optimizará recursos y superará obstáculos éticos asociados a otros sistemas animales. Su adopción generalizada podría marcar un punto de inflexión en la lucha contra neoplasias complejas.
REFERENCIAS BIBLIOGRÁFICAS
1. Sanz JM, Lahoz AG, Silva A. El sistema inmune y el microambiente tumoral: componentes y función [Internet]. Med - Programa Form Médica Contin Acreditado. 2021; 13(33):1932-41. DOI: https://doi.org/10.1016/j.med.2021.05.006
2. Hu C, Sun L, Chen J, Lyu Z, Yuan C, Jiang X. Advantages of the zebrafish tumor xenograft model: the evaluation of efficacy in cancer therapy and the application to the study of lncRNAs [Internet]. Front Immunol. 2024; 15:1483192. DOI: 10.3389/fimmu.2024.1483192
3. Offringa R, Kötzner L, Huck B, Urbahns K. The expanding role for small molecules in immuno-oncology [Internet]. Nat Rev Drug Discov. 2022;21(11):821-40. DOI: 10.1038/s41573-022-00538-9
4. Alnefaie A, Albogami S, Asiri Y, Ahmad T, Alotaibi SS, Al-Sanea MM, et al. Chimeric Antigen Receptor T-Cells: An Overview of Concepts, Applications, Limitations, and Proposed Solutions [Internet]. Front Bioeng Biotechnol. 2022; 10:797440. DOI: 10.3389/fbioe.2022.797440
5. Fazio M, Ablain J, Chuan Y, Langenau DM, Zon LI. Zebrafish patient avatars in cancer biology and precision cancer therapy [Internet]. Nat Rev Cancer. 2020;20(5):263-73. DOI: 10.1038/s41568-020-0252-3
6. Singh V, Khan N, Jayandhara GR. Vector engineering, strategies and targets in cancer gene therapy [Internet]. Cancer Gene Ther. 2021; 29(5): 402-17. DOI: 10.1038/s41417-021-00331-7
7. Esteva FJ, Hubbard-Lucey VM, Tang J, Pusztai L. Immunotherapy and targeted therapy combinations in metastatic breast cancer [Internet]. Lancet Oncol. 2019;20(3):e175-86. DOI: 10.1016/S1470-2045(19)30026-9
8. Xia Y, Du Z, Wang X, Li X. Treatment of uterine sarcoma with rAd-p53 (gendicine) followed by chemotherapy: clinical study of TP53 gene therapy [Internet]. Hum Gene Ther. 2018;29(2):242-50. DOI: https://doi.org/10.1089/hum.2017.206
9. Lazzari C, Spagnolo CC, Ciappina G, Di Pietro M, Squeri A, Passalacqua MI, et al. Immunotherapy in Early-Stage Non-Small Cell Lung Cancer (NSCLC): Current Evidence and Perspectives [Internet]. Curr Oncol. 2023;30(4): 3684-96. DOI: 10.3390/curroncol30040280
10. Zu H, Gao D. Non-viral Vectors in Gene Therapy: Recent Development, Challenges, and Prospects [Internet]. AAPS J. 2021;23(4):78. DOI: 10.1208/s12248-021-00608-7
11. Itez GG, Sunguroğlu A. CAR-T Therapy in Multiple Myeloma: Beyond Prejudice, Towards Value [Internet]. MDPI AG (Preprint). 2025: [aprox. 23 p]. DOI: https://doi.org/10.20944/preprints202509.2132.v1
12. Song G, Qi X, Zhao Y. iRGD Tumor Penetrating Peptide-Modified NK Cells Exhibit Enhanced Tumor Immune Infiltration Ability and Anti-Tumor Efficacy [Internet]. Protein Pept Lett. 2025;32(3):183-93. DOI: https://doi.org/10.2174/0109298665348639250115113650
13. Wawruszak A, Okoń E, Dudziak K. Advancements in Zebrafish Models for Breast Cancer Research: Unveiling Biomarkers, Targeted Therapies, and Personalized Medicine [Internet]. Med Sci Monit. 2023;29:e940550. DOI: 10.12659/MSM.940550
14. Astell KR, Sieger D. Zebrafish In Vivo Models of Cancer and Metastasis [Internet]. Cold Spring Harb Perspect Med. 2020; 10(10):a037077. DOI: 10.1101/cshperspect.a037077
15. Gautam MK, Panda PK, Dubey A, Kumari M, Ghosh NS. Zebrafish as a Fascinating Animal Model: A Robust Platform for in vivo Screening for Biomedical Research. Int J Pharm Investig. 2024; 14(3):681-92. DOI: 10.5530/ijpi.14.3.80
16. Pishas KI, Lessnick SL. Recent Advances in Targeted Therapy for Ewing Sarcoma. F1000Res. 2016;5: F1000 Faculty Rev-2077. [Version 1]. DOI: 10.12688/f1000research.8631.1
17. Cabezas-Sáinz P, Pensado-López A, Sáinz B, Sánchez L. Modeling cancer using zebrafish xenografts: Drawbacks for mimicking the human microenvironment [Internet]. Cells. 2020; 9(9):1978. DOI: https://doi.org/10.3390/cells9091978
18. Ferrero G, Gomez E, Lyer S, Rovira M, Miserocchi M, Langenau DM, et al. The macrophage-expressed gene (mpeg) 1 identifies a subpopulation of B cells in the adult zebrafish [Internet]. J Leukoc Biol. 2020; 107(3):431-43. DOI: https://doi.org/10.1002/JLB.1A1119-223R
19. Hall C, Flores M, Storm T, Croster K, Croster P. The zebrafish lysozyme C promoter drives myeloid-specific expression in transgenic fish [Internet]. BMC Dev Biol. 2007; 7:42. DOI: https://doi.org/10.1186/1471-213X-7-42
20. Sullivan C, Jurriens D, Sipkens J, Nguyen K, Hurlstone A, Brugman S. Zebrafish: an emerging model to study the cellular dynamics of inflammation in development, regeneration, and disease [Internet]. Front Cell Dev Biol. 2023; 10:1102381. DOI: 10.3389/fcell.2022.1102381
21. Yan C, Brunson DC, Tang Q, Do D, Iftimia NA, Moore JC, et al. Visualizing engrafted human cancer and therapy responses in immunodeficient zebrafish [Internet]. Cell. 2019; 177(7):1903-14.e14. DOI: https://doi.org/10.1016/j.cell.2019.04.004
22. Dudziak K, Nowak M, Sozoniuk M. One host-multiple applications: Zebrafish (Danio rerio) as promising model for studying human cancers and pathogenic diseases [Internet]. Int J Mol Sci. 2022; 23(18):10255. DOI: https://doi.org/10.3390/ijms231810255
23. Facchinello N, Schiavone MG, Al-Hamaly MA, Antonelli L, Tiso N, Gioacchini G, et al. Zebrafish cancer avatars: A translational platform for analyzing tumor heterogeneity and predicting patient outcomes [Internet]. Int J Mol Sci. 2023; 24(3):2288. DOI: https://doi.org/10.3390/ijms24032288
24. Robertson AL, Yue L, Choudhuri A, Kubaczka C, Wattrus SJ, Mandelbaum J, et al. Hematopoietic stem cell division is governed by distinct RUNX1 binding partners [Internet]. bioRxiv [Preprint]. 2024. DOI: 10.1101/2024.06.07.596542
25. Miao K, Kim G, Meara G, Qin X, Feng H. Tipping the Scales With Zebrafish to Understand Adaptive Tumor Immunity [Internet]. Front Cell Dev Biol. 2021; 9:660969. DOI: 10.3389/fcell.2021.660969
26. Tian HF, Xing J, Tang XQ, Chi H, Sheng XZ, Zhan WB. Cluster of differentiation antigens: essential roles in the identification of teleost fish T lymphocytes [Internet]. Mar Life Sci Technol. 2022;4(3):303-16. DOI: 10.1007/s42995-022-00136-z
27. Cariati M, Marlow R, Dontu G. Xenotransplantation of Breast Cancers Cancer cell culture [Internet]. Methods Mol Biol. 2011; 731:471-82. DOI: https://doi.org/10.1007/978-1-61779-080-5_38
28. Chen X, Li Y, Wang Z, Zhang H, Liu J, Wu S, et al. Benefits of zebrafish xenograft models in cancer research [Internet]. Front Cell Dev Biol. 2021;9:616551. DOI: 10.3389/fcell.2021.616551
29. Barbosa GR, de Souza AM, Silva PF, Fávero CS, de Oliveira JL, Carvalho HF, et al. Zebrafish as a Model for Translational Immuno-Oncology [Internet]. J Pers Med. 2025; 15(7):304. DOI: 10.3390/jpm15070304
30. Xiao J, Glasgow E, Agarwal S. Zebrafish xenografts for drug discovery and personalized medicine [Internet]. Trends Cancer. 2020; 6(7):569-79. DOI: 10.1016/j.trecan.2020.03.012
31. Lee LM, Seftor EA, Bonde G, Cornell RA, Hendrix MJ. The fate of human malignant melanoma cells transplanted into zebrafish embryos: assessment of migration and cell division in the absence of tumor formation [Internet]. Dev Dyn. 2005; 233(4):1560-70. DOI: 10.1002/dvdy.20471
32. Stoletov K, Montel V, Lester RD, Gonias SL, Klemke R. High-resolution imaging of the dynamic tumor cell-vascular interface in transparent zebrafish [Internet]. Proc Natl Acad Sci U S A. 2007; 104(44):17406-11. DOI: https://doi.org/10.1073/pnas.0703446104
33. Haldi M, Ton C, Seng WL, McGrath P. Human melanoma cells transplanted into zebrafish proliferate, migrate, produce melanin, form masses and stimulate angiogenesis in zebrafish [Internet]. Angiogenesis. 2006;9(3):139-51. DOI: 10.1007/s10456-006-9040-2
34. Veinotte CJ, Dellaire G, Berman JN. Hooking the big one: the potential of zebrafish xenotransplantation to reform cancer drug screening in the genomic era [Internet]. Dis Model Mech. 2014; 7(7):745-54. DOI: 10.1242/dmm.015784
35. Pascoal S, Salzer B, Scheuringer E, Wenninger-Weinzierl A, Sturtzel C, Holter W, et al. A preclinical embryonic zebrafish xenograft model to investigate CAR T cells in vivo [Internet]. Cancers (Basel). 2020; 12(3):567. DOI: https://doi.org/10.3390/cancers12030567
36. Fior R, Póvoa V, Mendes RV, Carvalho T, Gomes A, Figueiredo N, et al. Single-cell functional and chemosensitive profiling of combinatorial colorectal therapy in zebrafish xenografts. Proc Natl Acad Sci USA. 2017; 114(39):E8234-E8243. DOI: https://doi.org/10.1073/pnas.1618389114
37. Cabezas-Sainz P, Lago-Baameiro N, Vázquez-Ríos AJ, Piñeiro R, Pensado-López A, Bravo SB, et al. Morphological abnormalities and gene expression changes caused by high incubation temperatures in zebrafish xenografts with human cancer cells [Internet]. Genes (Basel). 2021;12(1):113. DOI: 10.3390/genes12010113
38. Chaudhary KR, Kinslow CJ, Cheng H, Silva JM, Yu J, Wang TJ, et al. Smurf2 inhibition enhances chemotherapy and radiation sensitivity in non-small-cell lung cancer [Internet]. Sci Rep. 2022;12(1):10140. DOI: 10.1038/s41598-022-14448-8
39. Khatib TO, Pedro BA, Bombin S, Matsuk VY, Robinson IE, Webster SF, et al. TGF-β1-mediated intercellular signaling fuels cooperative cellular invasion [Internet]. Cell Rep. 2025;44(2):115315. DOI: 10.1016/j.celrep.2025.115315
40. Cai W, Fan T, Xiao C, Deng Z, Liu Y, Li c, et al. Neutrophils in cancer: At the crucial crossroads of anti‐tumor and pro‐tumor. Cancer Communications, 2025; 45(8):888-913. DOI: 10.1002/cac2.70027
41. Kanthirigala SK, Palle K, Palle K. Engineered nanoparticle systems targeting tumor angiogenesis: bridging molecular mechanisms and therapeutic innovations [Internet]. Biomater Sci. 2026;14(3):215-30. DOI: 10.1039/D5BM01787D
42.Nicoli S, Ribatti D, Cotelli F, Presta M. Mammalian tumor xenografts induce neovascularization in zebrafish embryos [Internet]. Cancer Res. 2007; 67(7):2927-31. DOI: 10.1158/0008-5472.CAN-06-4268
43. Pruvot B, Jacquel A, Droin N, Auberger P, Bouscary D, Tamburini J, et al. Leukemic cell xenograft in zebrafish embryo for investigating drug efficacy [Internet]. Haematologica. 2011; 96(4):612-6. DOI: 10.3324/haematol.2010.031401
44. Emminger D. YB-1 drives aggressive behavior of mesothelioma cells and YB-1 inhibition sensitizes mesothelioma cells to chemotherapy [Internet]. [Tesis doctoral]. Universidad Veterinaria de Viena; 2020. Disponible en: https://phaidra.vetmeduni.ac.at/detail/o:1528
45. Yin J, Cao Y, He S, Huang Z, Wang Y, Zhang L, et al. Zebrafish patient-derived xenograft model as a preclinical platform for uveal melanoma drug discovery [Internet]. Pharmaceuticals (Basel). 2023;16(4):598. DOI: 10.3390/ph16040598
46. Wang X, Liu Y, Zhang H, Chen Z, Li J, Yang S, et al. Zebrafish xenograft model for studying pancreatic cancer-instructed innate immune microenvironment [Internet]. Int J Mol Sci. 2022;23(12):6442. DOI: 10.3390/ijms23126442
47. Asokan N, Daetwyler S, Bernas SN, Schmied C, Vogler S, Lambert K, et al. Long-term in vivo imaging reveals tumor-specific dissemination and captures host tumor interaction in zebrafish xenografts [Internet]. Sci Rep. 2020;10(1):13254. DOI: 10.1038/s41598-020-69956-2
48. Ritch SJ, Telleria CM. The transcoelomic ecosystem and epithelial ovarian cancer dissemination [Internet]. Front Endocrinol (Lausanne). 2022;13:886533. DOI: 10.3389/fendo.2022.886533
49. Ai X, Ye Z, Xiao B, Zhang Y, Chen Q, Xu J, et al. Clinically relevant orthotopic xenograft models of patient-derived glioblastoma in zebrafish. Dis Model Mech. 2022;15(4):49109. DOI: 10.1242/dmm.049109
50. Gaudenzi G, Vitale G. Transplantable zebrafish models of neuroendocrine tumors [Internet]. Ann Endocrinol (Paris). 2019;80 (3):149-52. DOI: 10.1016/j.ando.2019.04.005
51. Vargas-Patron LA, Agudelo-Dueñas N, Madrid-Wolff J, Venegas JA, González JM, Forero-Shelton M, et al. Xenotransplantation of Human glioblastoma in Zebrafish larvae: in vivo imaging and proliferation assessment [Internet]. Biol Open. 2019; 8(5):43257. DOI: https://doi.org/10.1242/bio.043257
52. Bottiglione F, Dee CT, Lea R, Zeef LAH, Badrock AP, Wane M, et al. Zebrafish IL-4-like cytokines and IL-10 suppress inflammation but only IL-10 is essential for gill homeostasis [Internet]. J Immunol. 2020;205(4):994-1008. DOI: 10.4049/jimmunol.2000295
53. Byrne AT, Alférez DG, Amant F, Annibali D, Arribas J, Biankin AV, et al. Interrogating open issues in cancer precision medicine with patient-derived xenografts [Internet]. Nat Rev Cancer. 2017;17(4):254-68. DOI: 10.1038/nrc.2016.140
54. Patton EE, Zon LI, Langenau DM. Zebrafish disease models in drug discovery: from preclinical modelling to clinical trials [Internet]. Nat Rev Drug Discov. 2021; 20(8):611-28. DOI: https://doi.org/10.1038/s41573-021-00210-8
55. Jin Y, Wei L, Jiang Q, Song X, Teng C, Fan C, et al. Comparison of efficacy and toxicity of bevacizumab, endostar and apatinib in transgenic and human lung cancer xenograft zebrafish model [Internet]. Sci Rep. 2018; 8(1):15837. DOI: https://doi.org/10.1038/s41598-018-34030-5
56. Miyawaki I. Application of zebrafish to safety evaluation in drug discovery [Internet]. J Toxicol Pathol. 2020;33(4):197-210. DOI: 10.1293/tox.2020-0027
57. Murali Shankar N, Ortiz-Montero P, Kurzyukova A, Rackwitz W, Künzel SR, Wels WS, et al. Preclinical assessment of CAR-NK cell-mediated killing efficacy and pharmacokinetics in a rapid zebrafish xenograft model of metastatic breast cancer [Internet]. Front Immunol. 2023; 14:1254821. DOI: https://doi.org/10.3389/fimmu.2023.1254821
58. Yu Y, Cheng Q, Ji Y, Wang Z, Liu J, Zhang L, et al. Biomaterial-based gene therapy [Internet]. MedComm (Beijing). 2023;4(3):e259. DOI: 10.1002/mco2.259
59. Kutle I, Polten R, Hachenberg J, Zimmermann K, Schambach A, Morgan M, et al. Anti-Mesothelin CAR-NK cells as a novel targeted therapy against cervical cancer [Internet]. Front Immunol. 2024;15:1485461. DOI: 10.3389/fimmu.2024.1485461
60. Mittal M, Kumari A, Paul B, Varshney A, Bhavya, Saini A, et al. Challenges and opportunities of gene therapy in cancer [Internet]. OBM Genet. 2024;8(1):1-501. DOI: 10.21926/obm.genet.2401219
61. Mashima R, Takada S. Lipid nanoparticles: a novel gene delivery technique for clinical application [Internet]. Curr Issues Mol Biol. 2022;44(10):5013-27. DOI: 10.3390/cimb44100341
62. Zhou Z, Liu X, Zhu D, Wang Y, Zhang Z, Zhou X, et al. Nonviral cancer gene therapy: Delivery cascade and vector nanoproperty integration [Internet]. Adv Drug Deliv Rev. 2017; 115:115-54. DOI: https://doi.org/10.1016/j.addr.2017.07.021
63. Park CS, Oh S, Kim Y, Lee J, Park S, Choi J, et al. Applications of CRISPR technologies to the development of gene and cell therapy [Internet]. BMB Rep. 2024;57(1):2-11. DOI: 10.5483/BMBRep.2023-0192
64. Sheikh S, Ernst D, Keating A. Prodrugs and prodrug-activated systems in gene therapy [Internet]. Mol Ther. 2021;29(5):1716-28. DOI: 10.1016/j.ymthe.2021.04.006
65. Taghdir M, Mussolino C. Viral and non-viral systems to deliver gene therapeutics to clinical targets [Internet]. Int J Mol Sci. 2024;25(13):7333. DOI: 10.3390/ijms25137333
66. Gavas S, Quazi S, Karpinski TM. Nanoparticles for Cancer Therapy: Current Progress and Challenges [Internet]. Nanoscale Res Lett. 2021; 16(1):173. DOI: https://doi.org/10.1186/s11671-021-03628-6
67. Sueira MS, Santos ES, Araujo RL, Silva LF, Oliveira MC, Costa AL, et al. Oral toxicities associated with immunotherapy and targeted therapy in cancer treatment [Internet]. Oral Oncol Rep. 2025;13:100724. DOI: 10.1016/j.oor.2024.100724
68. Dailey GP, Crosby EJ, Hartman ZC. Cancer vaccine strategies using self-replicating RNA viral platforms [Internet]. Cancer Gene Ther. 2023;30(6):794-802. DOI: 10.1038/s41417-022-00499-6
69. Yoder KE, Rabe A, Fishel R, Larue RC, Fuchs JR, Skalka AM, et al. Strategies for targeting retroviral integration for safer gene therapy: advances and challenges [Internet]. Front Mol Biosci. 2021;8:662331. DOI: 10.3389/fmolb.2021.662331
70. Zhang J, Liu Y, Zang M, Zhu S, Chen B, Li S, et al. Lentivirus mediated CDglyTK gene-modified free flaps by intra-artery perfusion show targeted therapeutic efficacy in rat model of breast cancer [Internet]. BMC Cancer. 2019; 19(1):1-11. DOI: https://doi.org/10.1186/s12885-019-6111-5
71. Mokkapati S, Narayan VM, Manyam GC, Lim AH, Duplisea JJ, Kokorovic A, et al. Lentiviral interferon: a novel method for gene therapy in bladder cancer [Internet]. Mol Ther Oncolytics. 2022;26:141-57. DOI: 10.1016/j.omto.2022.06.005
72. Manchon E, Hirt N, Versier B, Soundiramourty A, Juricek L, Lebbe C, et al. Harnessing nutrient scarcity for enhanced CAR-T-cell potency and safety in solid tumors [Internet]. Cell Mol Immunol. 2025; 22, 645–660. DOI: 10.1038/s41423-025-01290-x
73. Tseha ST. Role of adenoviruses in cancer therapy [Internet]. Front Oncol. 2022; 12:772659. DOI: 10.3389/fonc.2022.772659
74. Ehrke-Schulz E, Heinemann S, Schulte L, Schiwon M, Ehrhardt A. Adenoviral vectors armed with PAPILLOMAVIRUS oncogene specific CRISPR/Cas9 kill human-papillomavirus-induced cervical cancer cells [Internet]. Cancers (Basel). 2020; 12(8):1934. DOI: https://doi.org/10.3390/cancers12071934
75. Byrne BJ, Flanigan KM, Matesanz SE, Finkel RS, Waldrop MA, D'Ambrosio ES, et al. Current clinical applications of AAV-mediated gene therapy [Internet]. Mol Ther. 2025; 33(6):2479-516. DOI: 10.1016/j.ymthe.2025.04.045
76. Wang JH, Gessler DJ, Zhan W, Gallagher TL, Gao G. Adeno-associated virus as a delivery vector for gene therapy of human diseases [Internet]. Signal Transduct Target Ther. 2024;9(1):78. DOI: 10.1038/s41392-024-01780-w
77. Maksimov DO, Naumova DA, Astakhova EA, Artemev VV, Biryukov SA, Abramov IS, et al. In vivo evaluation of tropism and biodistribution of synthetic and natural adeno-associated viral vectors by next-generation sequencing [Internet]. Biopreparados: Prevención, diagnóstico y tratamiento.. 2024; 24(2):215-28. DOI: 10.30895/2221-996X-2024-24-2-215-228
78. Sung YK, Kim SW. Recent advances in the development of gene delivery systems [Internet]. Biomater Res. 2019; 23(1):8. DOI: 10.1186/s40824-019-0156-z
79. Santana-Armas ML, Tros de Ilarduya C. Strategies for cancer gene-delivery improvement by non-viral vectors [Internet]. Int J Pharm. 2021;596:120291. DOI: 10.1016/j.ijpharm.2021.120291
80. Jiang C, Chen J, Li Z, Wang Z, Zhang W, Liu J. Recent advances in the development of polyethylenimine-based gene vectors for safe and efficient gene delivery [Internet]. Expert Opin Drug Deliv. 2019; 16(4):363-76. DOI: 10.1186/s40824-019-0156-z
81. Luo X, Wen W. MicroRNA in prostate cancer: from biogenesis to applicative potential [Internet]. BMC Urol. 2024;24(1):244. DOI: 10.1186/s12894-024-01634-1
82. Habibizadeh M, Lotfollahzadeh S, Mahdavi P, Mohammadi S, Tavallaei O. Nanoparticle-mediated gene delivery of TRAIL to resistant cancer cells: a review [Internet]. Heliyon. 2024;10(16):e36057. DOI: 10.1016/j.heliyon.2024.e36057
83. Baig B, Halim SA, Farrukh A, Greish Y, Amin A. Current status of nanomaterial-based treatment for hepatocellular carcinoma [Internet]. Biomed Pharmacother. 2019; 116:108852. DOI: https://doi.org/10.1016/j.biopha.2019.108852
84. Li D, Gao C, Kuang M, Xu M, Wang B, Luo Y, et al. Nanoparticles as drug delivery systems of RNAi in cancer therapy [Internet]. Molecules. 2021;26(8):2380. DOI: 10.3390/molecules26082380
85. Diep YN, Kim TJ, Cho H, Lee LP. Nanomedicine for advanced cancer immunotherapy [Internet]. J Control Release. 2022; 351:1017-37. DOI: https://doi.org/10.1016/j.jconrel.2022.10.004
86. Mohammad-Hadi L, Mohammad-Hadi M. 3D in vitro cancer models [Internet]. In: Mohammad-Hadi L, Mohammad-Hadi M. Applications of minimally invasive nanomedicine-based therapies in 3D in vitro cancer platforms. Cham: Springer; 2021. p. 85-102. DOI: https://doi.org/10.1007/978-3-031-02388-0_5
87. Ueda Y, Kawamoto K, Konno M, Noguchi K, Kaifuchi S, Satoh T, et al. Application of C. elegans cancer screening test for the detection of pancreatic tumor in genetically engineered mice [Internet]. Oncotarget. 2019; 10(53):5412-8. DOI: 10.18632/oncotarget.27124
88. Hason M, Bartůnĕk P. Zebrafish models of cancer-new insights on modeling human cancer in a non-mammalian vertebrate [Internet]. Genes (Basel). 2019; 10(11):1-30. DOI: https://doi.org/10.3390/genes10110935
89. Sharpe JL, Morgan J, Poon C, Tian A, Bruckner K, Richardson HE. Modelling cancer metastasis in Drosophila melanogaster [Internet]. Cells. 2023;12(5):677. DOI: 10.3390/cells12050677
90. Bosenberg M, Merlino G, Chen Q, Liu Y, Patel S, Zhou X, et al. Mouse models for immuno-oncology [Internet]. Trends Cancer. 2023;9(7):578-90. DOI: 10.1016/j.trecan.2023.03.010
91. Horzmann KA, Freeman JL. Making waves: New developments in toxicology with the zebrafish [Internet]. Toxicol Sci. 2018; 163(1):5-12. DOI: https://doi.org/10.1093/toxsci/kfy044
92. Pensado-López A, Fernández-Rey J, Reimunde P, Crecente-Campo J, Sánchez L, Alonso MJ, et al. Zebrafish models for the safety and therapeutic testing of nanoparticles with a focus on macrophages [Internet]. Nanomaterials (Basel). 2021;11(7):1784. DOI: 10.3390/nano11071784
93. Al-Thani HF, Shurbaji S, Yalcin HC. Zebrafish as a model for anticancer nanomedicine studies [Internet]. Pharmaceuticals (Basel). 2021; 14(7):625. DOI: https://doi.org/10.3390/ph14070625
Conflictos de interés
Los autores declaran que no existe ningún conflicto de interés financiero o personal de ningún tipo que pudiera influir en el desarrollo, las conclusiones o la publicación de esta revisión.
Contribuciones de los autores
Conceptualización: Yanier Núñez Figueredo, Ché Serguera.
Curación de datos: Anabel Cisnero Campo, Sonia García Lago.
Análisis Formal: Kamila Morín Fanego, Silvia García Viamonte.
Supervisión: Dianelys Cabrera Fonseca, Yenia Aldana Mulet.
Redacción - Elaboración del borrador original: Thalía Sánchez Miralles.
Redacción - Revisión y edición: Sheyla Fernández Puentes, Yanier Núñez Figueredo, Thalía Sánchez Miralles.
Declaración de disponibilidad de datos
Archivo complementario: resumen gráfico del estudio (PDF). Disponible en: https://revmedmilitar.sld.cu/index.php/mil/libraryFiles/downloadPublic/157